熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
能量應(yīng)激反應(yīng)途徑。
為了測(cè)試SDS細(xì)胞利用哪些代償機(jī)制來(lái)抵消能量生產(chǎn)缺陷(能量應(yīng)激),我們?cè)u(píng)估了AMP激活蛋白激酶(AMPK)和PI3K/AKT/哺乳動(dòng)物雷帕霉素靶標(biāo)(mTOR)通路,它們是能量缺乏激活的主要調(diào)節(jié)機(jī)制。
在應(yīng)激條件下,AMPK通過(guò)AMP積累被激活,拮抗mTOR并刺激糖酵解等替代性分解代謝過(guò)程,從而抵消能量限制。PI3K/AKT/mTOR通路通過(guò)線粒體和核糖體的生物生成誘導(dǎo)細(xì)胞增殖。被PI3K(磷脂酰肌醇3-激酶)在Thr803處磷酸化的AKT會(huì)抑制AMPK并誘導(dǎo)mTOR激活。因此,在野生型細(xì)胞中,當(dāng)AMPK被激活時(shí),PI3K/AKT/mTOR通路通常會(huì)受到抑制。
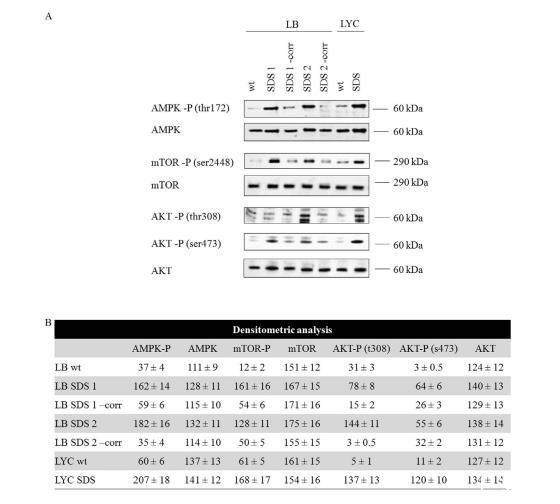
如預(yù)期的那樣,在SDS細(xì)胞中,AMPK比對(duì)照組更活躍,如蛋白磷酸化形式的Western印跡分析所示(圖3)。令人驚訝的是,我們發(fā)現(xiàn)與正常對(duì)照組和校正對(duì)照組相比,mTOR并未受到抑制,反而高度磷酸化。
與這一發(fā)現(xiàn)相一致的是,我們發(fā)現(xiàn)與野生型細(xì)胞和校正細(xì)胞相比,SDS細(xì)胞中AKT在Thr803和Ser473處也過(guò)度磷酸化,從而證實(shí)了整個(gè)PI3K/AKT/mTOR通路的過(guò)度激活。
總之,這些實(shí)驗(yàn)表明,SDS細(xì)胞對(duì)高能應(yīng)激反應(yīng)異常,而這種反應(yīng)與SDS蛋白有關(guān),因?yàn)樵谛U?xì)胞中未見(jiàn)PI3K/AKT/mTOR通路超活化。
SDS細(xì)胞的細(xì)胞質(zhì)鈣濃度水平很高。
Ca2+調(diào)節(jié)真核蛋白質(zhì)翻譯和許多其他消耗ATP的細(xì)胞反應(yīng),因此是蛋白質(zhì)合成和能量代謝的重要信號(hào)分子。此外,高[Ca2+]i與ROS細(xì)胞毒性、脂質(zhì)過(guò)氧化和OXPHOS功能密切相關(guān),并且會(huì)抑制復(fù)合體IV的活性。
在靜息狀態(tài)下,SDS細(xì)胞的[Ca2+]i比野生型細(xì)胞(65±2nM)或校正細(xì)胞(64±1nM)高出兩倍(133±8nM)(表1)。
為了研究[Ca2+]i增高的原因,我們?cè)u(píng)估了ER從細(xì)胞質(zhì)中捕獲并儲(chǔ)存鈣的能力。事實(shí)上,ER是細(xì)胞內(nèi)主要的鈣儲(chǔ)存場(chǎng)所,并通過(guò)SERCA(鈣ATP酶通道)活性在Ca2+穩(wěn)態(tài)中發(fā)揮重要作用,SERCA可將Ca2+從細(xì)胞質(zhì)轉(zhuǎn)移到ER。硫代碳酸氫鹽(TG)不可逆地阻斷SERCA通道,導(dǎo)致Ca2+從ER泄漏,從而增加[Ca2+]i。與SDS細(xì)胞相比,高劑量TG處理(3μM)會(huì)導(dǎo)致野生型細(xì)胞和校正細(xì)胞中的[Ca2+]i顯著增加,從而表明這些細(xì)胞在ER中儲(chǔ)存Ca2+的能力受損,這可能是[Ca2+]i增加的原因(表1)。
盡管我們沒(méi)有發(fā)現(xiàn)任何SERCA通道活性差異,但我們推測(cè)[Ca2+]i的增加可能取決于我們?cè)赟DS細(xì)胞中觀察到的mTOR激活,已知mTOR可通過(guò)肌醇-1,4,5三磷酸受體正向調(diào)節(jié)鈣釋放。
亮氨酸可恢復(fù)正常代謝表型。
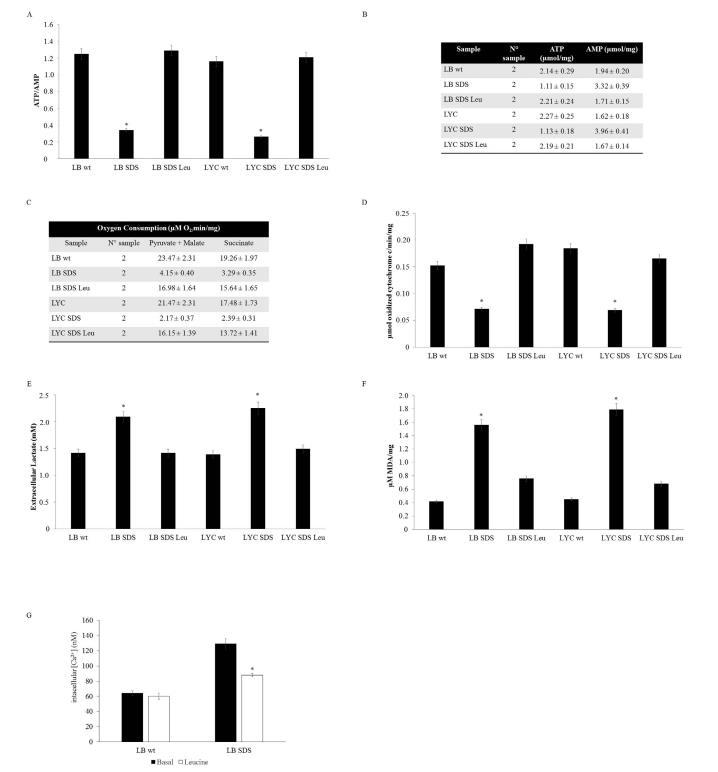
由于亮氨酸(Leucine,Leu)是一種已知能促進(jìn)蛋白質(zhì)合成的必需氨基酸,即使在SBDS缺乏的細(xì)胞中也是如此,因此我們測(cè)試了亮氨酸在處理5天后對(duì)SDS淋巴細(xì)胞和淋巴母細(xì)胞的生化影響。經(jīng)過(guò)Leu處理后,復(fù)合體IV的功能得到恢復(fù),呼吸速率和ATP/AMP比率與對(duì)照組相當(dāng)(圖4A-D),細(xì)胞內(nèi)鈣濃度也有所降低(圖4G)。表型逆轉(zhuǎn)還與脂質(zhì)過(guò)氧化和乳酸產(chǎn)生的減少有關(guān)(圖4E、F)。令人驚訝的是,用N-乙酰半胱氨酸(NAC)(一種抗氧化分子,是還原型谷胱甘肽的前體)處理后,在SDS細(xì)胞中觀察到的呼吸缺陷、能量窘迫和鈣平衡改變沒(méi)有恢復(fù)或恢復(fù)較差。
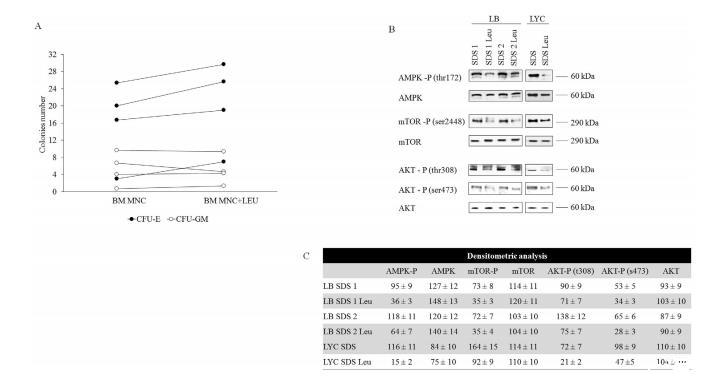
然后,我們測(cè)試了Leu對(duì)SDS患者骨髓造血干細(xì)胞生長(zhǎng)的影響,觀察到紅細(xì)胞集落生長(zhǎng)適度增加,但髓系細(xì)胞集落生長(zhǎng)沒(méi)有增加(圖5A)。由于Leu是mTOR激活的調(diào)節(jié)劑,我們研究了它在慢性SDS細(xì)胞處理后對(duì)能量應(yīng)激途徑的影響。不出所料,AMPK磷酸化的減少是正常OXPHOS恢復(fù)的結(jié)果。有趣的是,Leu處理后AKT和mTOR磷酸化水平也降低了(圖5B)。可以推測(cè)這些影響是由于依賴于營(yíng)養(yǎng)過(guò)剩的AKT/mTOR通路的反饋調(diào)節(jié)所致。說(shuō)明Leu恢復(fù)了SDS細(xì)胞的生化表型,該分子可被視為恢復(fù)SDS細(xì)胞能量代謝的潛在工具。
討論
SBDS蛋白在核糖體生物生成和蛋白質(zhì)合成過(guò)程中發(fā)揮作用,而這兩個(gè)高耗能過(guò)程與細(xì)胞能量的產(chǎn)生密切相關(guān)。細(xì)胞呼吸是將營(yíng)養(yǎng)物質(zhì)轉(zhuǎn)化為生化能量(主要是ATP)的一系列代謝反應(yīng)和過(guò)程。這一過(guò)程由一系列稱為電子傳遞鏈的蛋白質(zhì)復(fù)合物完成,電子傳遞鏈位于線粒體內(nèi)膜,并與線粒體膜間隙和基質(zhì)相連。呼吸功能受損會(huì)影響ATP的產(chǎn)生,并使細(xì)胞面臨能量和氧化壓力。
在本研究中,我們?cè)u(píng)估了SDS細(xì)胞的能量代謝,發(fā)現(xiàn)在丙酮酸/蘋果酸或琥珀酸的誘導(dǎo)下,氧消耗會(huì)受損。因此,ATP生成減少,AMP積累,從而改變了ATP/AMP比率。
電子通過(guò)兩條途徑傳輸。第一種由復(fù)合物I、III和IV組成,從NADH中轉(zhuǎn)移電子,可由丙酮酸/蘋果酸誘導(dǎo)。另一種需要復(fù)合體II、III和IV,由琥珀酸激活,從FADH2中轉(zhuǎn)移電子,能量產(chǎn)生效率低于第一種途徑。由于丙酮酸/蘋果酸和琥珀酸在SDS細(xì)胞中對(duì)耗氧量的影響程度相同,我們對(duì)兩種途徑共有的兩個(gè)復(fù)合物(III和IV)的活性進(jìn)行了研究,結(jié)果表明復(fù)合物IV不能正常工作。
復(fù)合體IV活性受損的原因尚不清楚。我們?cè)u(píng)估了分別由核基因和線粒體基因編碼的復(fù)合體IV的兩個(gè)亞基COX5A和COX2的表達(dá)水平,發(fā)現(xiàn)這兩種蛋白的表達(dá)水平正常。這表明,盡管SDS細(xì)胞中存在核糖體生物發(fā)生和轉(zhuǎn)導(dǎo)缺陷,但它們的合成并沒(méi)有受損。不過(guò),值得注意的是,復(fù)合體IV由32個(gè)蛋白質(zhì)組成,其中3個(gè)由線粒體DNA編碼,29個(gè)由核DNA編碼。此外,其中11個(gè)是結(jié)構(gòu)蛋白,18個(gè)是組裝因子;因此,我們不能排除其他亞基表達(dá)較少或折疊不正確的可能性。
另一個(gè)原因可能是線粒體膜發(fā)生了變化,這是由復(fù)合體III和IV之間或復(fù)合體IV與氧之間的電子傳遞發(fā)生變化所決定的,從而導(dǎo)致細(xì)胞色素c氧化酶活性受損,氧化應(yīng)激增加。然而,這種可能性似乎不大,因?yàn)槲覀冊(cè)赟DS細(xì)胞中測(cè)得的氧化應(yīng)激水平較低,并觀察到線粒體膜明顯完整。
值得注意的是,盡管復(fù)合體IV在ROS生成中起間接作用,但復(fù)合體IV的損傷可能是由復(fù)合體I和復(fù)合體III的上游電子累積引起的,從而導(dǎo)致ROS生成增加。事實(shí)上,線粒體電子傳遞鏈包含多個(gè)氧化還原中心,可直接將電子傳遞給氧氣,從而產(chǎn)生ROS。不過(guò),也可能有其他結(jié)構(gòu)參與了氧化應(yīng)激誘導(dǎo)。特別是,由于SDS細(xì)胞的特點(diǎn)是蛋白質(zhì)生物生成缺陷,缺陷蛋白質(zhì)的積累可能會(huì)導(dǎo)致內(nèi)質(zhì)網(wǎng)中的未折疊蛋白反應(yīng)。
復(fù)合體IV受損的另一個(gè)可能原因與所報(bào)道的SDS細(xì)胞中鈣水平的改變有關(guān)。細(xì)胞內(nèi)的鈣平衡在調(diào)控生化通路中發(fā)揮著重要作用,而生化通路可調(diào)節(jié)對(duì)高能應(yīng)激的反應(yīng)。特別是,Ca2+對(duì)能量代謝有雙重影響。一種作用是,[Ca2+]i可增強(qiáng)OXPHOS,從而激活克雷布斯循環(huán)脫氫酶和線粒體底物轉(zhuǎn)運(yùn)體。另一個(gè)作用是,[Ca2+]i可能通過(guò)競(jìng)爭(zhēng)復(fù)合體IV的陽(yáng)離子結(jié)合位點(diǎn)而影響其活性。
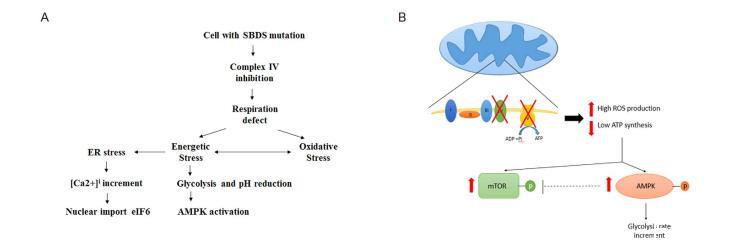
考慮到這些數(shù)據(jù)(圖6),在SDS細(xì)胞中觀察到的高[Ca2+]i可能與解釋SDS細(xì)胞的生化表型有關(guān)。SBDS與類延伸因子1(EFL1)合作,使eIF6從前60S核糖體亞基中釋放,從而形成核糖體80S。因此,在SDS細(xì)胞中,60S亞基的成熟是有缺陷的,其與40S亞基的結(jié)合也受到損害。此外,即使在細(xì)胞質(zhì)中,eIF6與前60S亞基的結(jié)合也會(huì)持續(xù)存在,阻止其循環(huán)到核仁。考慮到eIF6的核導(dǎo)入受細(xì)胞內(nèi)Ca2+的調(diào)節(jié),我們可以推測(cè),SDS細(xì)胞中細(xì)胞質(zhì)鈣濃度的增加試圖平衡核糖體生物發(fā)生的缺陷。
能量應(yīng)激會(huì)誘導(dǎo)細(xì)胞新陳代謝發(fā)生變化,從而刺激或抑制參與能量平衡調(diào)節(jié)的分子網(wǎng)絡(luò),如AMPK和mTOR。在觀察到的SDS細(xì)胞中,由于能量應(yīng)激,AMPK被過(guò)度激活,糖酵解途徑受到刺激。令人驚訝的是,我們還發(fā)現(xiàn)AKT/mTOR通路被異常地過(guò)度激活,因?yàn)檫@兩種蛋白都被過(guò)度磷酸化。我們推測(cè),mTOR過(guò)度激活是SDS細(xì)胞支持能量缺陷和蛋白質(zhì)合成的一種方式,目的是改善OXPHOS活性。然而,用mTOR拮抗劑雷帕霉素處理SDS細(xì)胞可完全抑制殘余的OXPHOS活性,從而減少ROS的產(chǎn)生,進(jìn)而通過(guò)糖酵解恢復(fù)能量。這表明,在SDS細(xì)胞生化改變的過(guò)程中,OXPHOS活性的增加在保證ATP產(chǎn)量增加的同時(shí),也可能導(dǎo)致氧化應(yīng)激的增強(qiáng)和細(xì)胞損傷的潛在增加(圖6)。在AMPK激活的情況下,mTOR激活的另一個(gè)潛在機(jī)制可能與自噬激活有關(guān)。在核糖體病中,氧化應(yīng)激的增加會(huì)通過(guò)mTOR-S6激酶途徑誘導(dǎo)自噬。考慮到本手稿中報(bào)告的數(shù)據(jù),我們可以假設(shè)AMPK活性增強(qiáng)可能與細(xì)胞能量狀態(tài)受損有關(guān),而mTOR通路激活可能與氧化應(yīng)激產(chǎn)生水平較高有關(guān)。
此外,mTOR還控制著幾個(gè)依賴Ca2+的過(guò)程。例如,它正向調(diào)節(jié)IP3R(三磷酸肌醇受體)介導(dǎo)的Ca2+釋放,并與Akt共同參與調(diào)節(jié)線粒體相關(guān)內(nèi)質(zhì)網(wǎng)膜(MAM)的完整性、鈣通量和能量代謝。
最后,糖酵解代謝的增加會(huì)引起乳酸的積累和細(xì)胞內(nèi)pH值的降低,從而導(dǎo)致鈣泵受到抑制,細(xì)胞膜[Ca2+]隨之增加(圖6)。
亮氨酸是一種必需氨基酸,能促進(jìn)細(xì)胞增殖和蛋白質(zhì)合成。核糖體病或其他核糖體生物發(fā)生缺陷的病癥可從這種氨基酸的治療中獲益。與這些研究一致,我們發(fā)現(xiàn)亮氨酸能改善SDS患者的體外紅細(xì)胞生成。此外,用亮氨酸處理SDS細(xì)胞可恢復(fù)OXPHOS和ATP合成,降低細(xì)胞質(zhì)鈣濃度以及AMPK和AKT/mTOR活性,這表明亮氨酸可能有助于維持SDS患者紊亂的能量代謝和紅細(xì)胞生成。特別是,考慮到亮氨酸能提高OXPHOS活性,部分恢復(fù)呼吸作用,因此它可能是AMPK和AKT/mTOR通路的調(diào)節(jié)劑,能恢復(fù)它們的生理作用。我們可以推測(cè),亮氨酸誘導(dǎo)的氧化應(yīng)激減少會(huì)導(dǎo)致mTOR-S6激酶途徑失活。
最后,值得注意的是,能量代謝是維持自我更新干細(xì)胞的決定因素。骨髓中的造血干細(xì)胞被封閉在缺氧的微環(huán)境中。缺氧條件使造血干細(xì)胞處于靜止?fàn)顟B(tài),這與糖酵解代謝有關(guān)。在(不對(duì)稱)自我更新干細(xì)胞分裂過(guò)程中,一個(gè)細(xì)胞保持干細(xì)胞的糖代謝特征,而另一個(gè)細(xì)胞則進(jìn)入血管,獲得OXPHOS代謝并進(jìn)行分化。造血干細(xì)胞對(duì)氧化應(yīng)激增加很敏感,而線粒體氧化磷酸化是產(chǎn)生ROS的主要原因。因此,糖酵解代謝是造血干細(xì)胞自我更新維持的決定因素。為了減少線粒體代謝,造血干細(xì)胞會(huì)積極調(diào)節(jié)AMPK,同時(shí)抑制PI3K/mTOR通路。AKT或mTOR信號(hào)的持續(xù)活躍和高[Ca2+]i水平會(huì)導(dǎo)致增殖增加和造血干細(xì)胞貧化。因此,這項(xiàng)研究可為了解導(dǎo)致SDS患者骨髓衰竭的生化途徑提供一個(gè)新的視角。
總之,我們首次發(fā)現(xiàn),盡管SDS細(xì)胞的線粒體形態(tài)沒(méi)有發(fā)生顯著變化,但它卻遭受著與SBSD蛋白缺陷有關(guān)的能量應(yīng)激和嚴(yán)重的呼吸缺陷。這些缺陷可通過(guò)增強(qiáng)的AMPK、糖酵解和mTOR/Akt通路激活得到部分補(bǔ)償。在維持這種改變的新陳代謝中起關(guān)鍵作用的可能是鈣平衡的改變。
 相關(guān)新聞
相關(guān)新聞