熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
阿爾茨海默病(Alzheimer's disease,AD),俗稱老年癡呆,是一種以記憶衰退和認(rèn)知功能進(jìn)行性下降為特征的神經(jīng)退行性疾病。隨著人口老齡化,我國(guó)AD患者預(yù)計(jì)到2050年將超過(guò)3000萬(wàn)例,給社會(huì)和家庭帶來(lái)沉重負(fù)擔(dān)。科學(xué)家發(fā)現(xiàn),這種病可能與大腦中一種叫"β-淀粉樣蛋白"的有害物質(zhì)堆積[1]以及大腦中多巴胺系統(tǒng)的失調(diào)[2-4]有關(guān)。但目前醫(yī)學(xué)界還沒(méi)有找到完全治愈的方法。現(xiàn)有的無(wú)創(chuàng)腦部電刺激治療雖然有一定效果,但存在兩個(gè)主要難題:一是難以精準(zhǔn)刺激到大腦深部的關(guān)鍵區(qū)域,二是無(wú)法實(shí)時(shí)監(jiān)測(cè)腦內(nèi)化學(xué)物質(zhì)的變化。此外,目前缺乏能夠同時(shí)實(shí)現(xiàn)精準(zhǔn)刺激和監(jiān)測(cè)的微型腦部治療設(shè)備。
在微納傳感技術(shù)創(chuàng)新研究群體和前沿交叉研判戰(zhàn)略研究聯(lián)合等項(xiàng)目支持下,中國(guó)科學(xué)院空天信息創(chuàng)新研究院(簡(jiǎn)稱“中科院空天院”)吳一戎/宋軼琳/蔡新霞團(tuán)隊(duì)在Nature Communications上發(fā)表了題為“Integrated dopamine sensing and 40 Hz hippocampal stimulation improves cognitive performance in Alzheimer’s mouse models”的最新研究成果,研發(fā)了一種雙模雙向柔性腦機(jī)接口神經(jīng)微電極NeuroRevive-FlexChip。集成多巴胺實(shí)時(shí)監(jiān)測(cè)、神經(jīng)電活動(dòng)記錄和原位電刺激功能,發(fā)現(xiàn)了40Hz微電流靶向刺激海馬區(qū)后,誘發(fā)AD小鼠海馬體神經(jīng)元多巴胺釋放和微觀神經(jīng)振蕩,改善AD小鼠認(rèn)知功能。研究發(fā)現(xiàn),采用NeuroRevive-FlexChip進(jìn)行40Hz電刺激,會(huì)誘發(fā)多巴胺水平短暫升高,并呈現(xiàn)刺激結(jié)束后短期重啟現(xiàn)象。在重啟期內(nèi),神經(jīng)元放電模式從簇狀放電(burst firing),轉(zhuǎn)變?yōu)槌掷m(xù)性放電(tonic firing)。最終,經(jīng)過(guò)治療的AD小鼠在Y迷宮測(cè)試中的認(rèn)知能力增強(qiáng);微觀神經(jīng)分子與細(xì)胞分析也證實(shí)該干預(yù)可有效減少Aβ42沉積,并誘導(dǎo)小膠質(zhì)細(xì)胞形態(tài)重塑。這一創(chuàng)新性技術(shù)實(shí)現(xiàn)了電生理-電化學(xué)雙模態(tài)檢測(cè)與神經(jīng)調(diào)控的器件集成,為AD的精準(zhǔn)干預(yù)和治療靶點(diǎn)尋找提供了技術(shù)平臺(tái)。該技術(shù)有望突破現(xiàn)有AD治療中深部腦區(qū)靶向性不足與多模式檢測(cè)缺失的技術(shù)瓶頸,為阿爾茨海默癥等難治性神經(jīng)疾病精準(zhǔn)治療提供新型腦機(jī)接口技術(shù)手段,具有重要的科學(xué)意義和臨床價(jià)值。
1.柔性神經(jīng)電極NeuroRevive-FlexChip實(shí)現(xiàn)多巴胺和神經(jīng)電活動(dòng)檢測(cè)與電刺激一體化
針對(duì)阿爾茨海默病中多巴胺信號(hào)紊亂與神經(jīng)放電異常并存的復(fù)雜病理,研究團(tuán)隊(duì)研發(fā)了NeuroRevive-FlexChip,這是一款柔性腦機(jī)接口神經(jīng)微電極,首次實(shí)現(xiàn)了在小鼠深腦海馬CA1區(qū)原位靶向刺激、神經(jīng)電活動(dòng)以及多巴胺濃度動(dòng)態(tài)釋放的一體化檢測(cè)。該神經(jīng)微電極采用雙導(dǎo)電層結(jié)構(gòu)設(shè)計(jì),包含高空間分辨率的微電極陣列。神經(jīng)微電極的電生理檢測(cè)阻抗低至2~3 kΩ1kHz,多巴胺檢測(cè)限達(dá)100 nM,檢測(cè)靈敏度約為37.54 pA/μM。
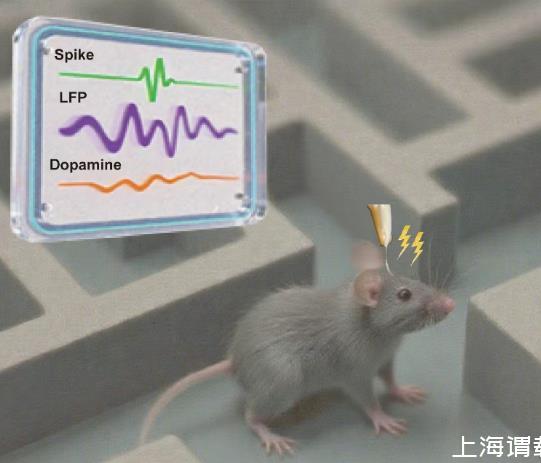
圖1深腦靶向刺激改善阿爾茨海默模型小鼠認(rèn)知功能
2.40Hz電刺激調(diào)控誘導(dǎo)多巴胺動(dòng)態(tài)釋放與微觀神經(jīng)振蕩,揭示神經(jīng)調(diào)控新機(jī)制
使用NeuroRevive-FlexChip對(duì)APP/PS1小鼠進(jìn)行海馬CA1區(qū)40Hz電刺激后,研究者觀察到一種顯著的“多巴胺重啟現(xiàn)象”:刺激期間多巴胺濃度迅速升高,刺激停止后先下降,隨后又自發(fā)回升。這種動(dòng)力學(xué)過(guò)程呈現(xiàn)出刺激后多巴胺釋放-回落-再上升的循環(huán),提示存在一個(gè)刺激觸發(fā)的短時(shí)調(diào)控回路。
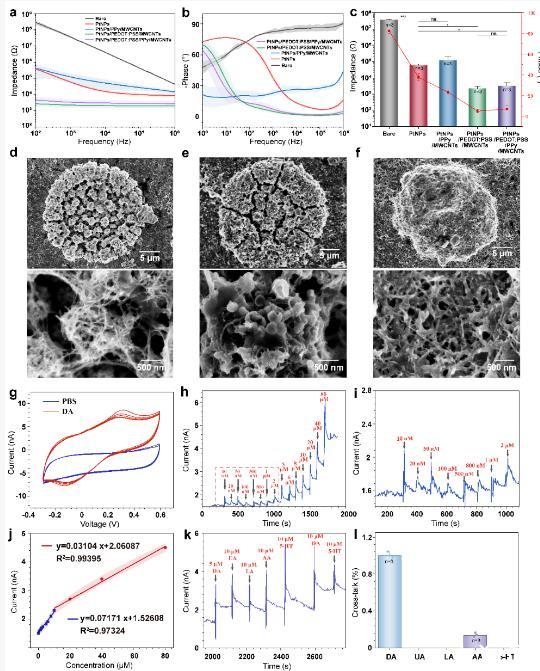
圖2.柔性腦機(jī)接口NeuroRevive-FlexChip的神經(jīng)電活動(dòng)和多巴胺檢測(cè)性能
與多巴胺濃度波動(dòng)相對(duì)應(yīng),神經(jīng)元放電模式也發(fā)生了轉(zhuǎn)換。具體而言,當(dāng)多巴胺水平下降時(shí),神經(jīng)元以稀疏、規(guī)律的持續(xù)性放電(tonic firing)為主;而在多巴胺濃度上升階段,神經(jīng)元?jiǎng)t出現(xiàn)簇狀放電(burst firing)。尤其在300μA刺激強(qiáng)度下,每一個(gè)5 s分布的簇中動(dòng)作電位的平均發(fā)放頻率接近8 Hz,而每一個(gè)簇中包含40個(gè)動(dòng)作電位,提示神經(jīng)元可能與刺激信號(hào)頻率發(fā)生了神經(jīng)協(xié)同效應(yīng)。這一現(xiàn)象揭示了電刺激—多巴胺釋放—放電模式重構(gòu)之間的動(dòng)態(tài)反饋機(jī)制,首次明確電生理調(diào)控可通過(guò)多巴胺介導(dǎo)的方式快速重塑神經(jīng)活動(dòng)節(jié)律。
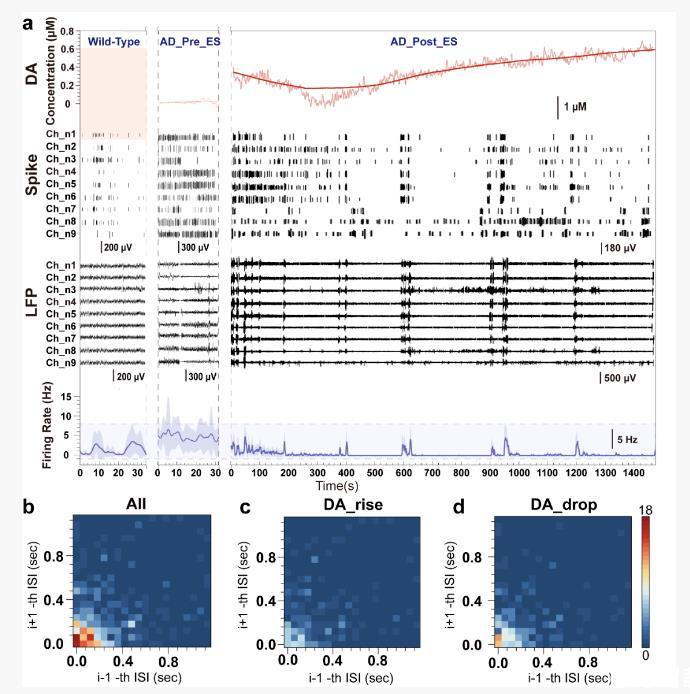
圖3.深腦靶向刺激引起多巴胺釋放和微觀神經(jīng)振蕩
3.多尺度驗(yàn)證電刺激改善AD病理的干預(yù)效果,建立從行為到分子的完整證據(jù)鏈
本研究通過(guò)從行為學(xué)、細(xì)胞電生理、神經(jīng)遞質(zhì)水平到組織病理學(xué)的多尺度驗(yàn)證,建立了電刺激調(diào)控AD病理機(jī)制的完整證據(jù)鏈。在宏觀行為層面,APP/PS1模型小鼠在40 Hz刺激后,其Y迷宮自發(fā)交替率由刺激前的47%提升至61%,接近野生型水平63%,說(shuō)明空間工作記憶有所改善。在微觀分子層面,刺激7天后的小鼠海馬CA1和DG區(qū)Aβ42斑塊顯著減少,說(shuō)明40 Hz電刺激可調(diào)控與AD核心病理相關(guān)的淀粉樣蛋白積累。此外,免疫組織化學(xué)顯示刺激后小鼠海馬區(qū)小膠質(zhì)細(xì)胞樹(shù)突數(shù)量、分支長(zhǎng)度、末端數(shù)量顯著增加,表明其可能在清除Aβ42過(guò)程中發(fā)揮積極作用。
藥理干預(yù)實(shí)驗(yàn)進(jìn)一步驗(yàn)證了多巴胺在這一效應(yīng)鏈條中的中介作用:使用多巴胺D2受體拮抗劑可完全阻斷40 Hz刺激誘導(dǎo)的多巴胺釋放與神經(jīng)放電改變,而D1/D2激動(dòng)劑可顯著提升多巴胺水平并誘導(dǎo)burst firing。
綜上,研究首次從電刺激—神經(jīng)遞質(zhì)—神經(jīng)活動(dòng)—病理改變—行為改善這一完整路徑,系統(tǒng)揭示了40 Hz刺激對(duì)AD病理的多層次干預(yù)潛力,為AD早期治療提供了新策略和多維證據(jù)支持。
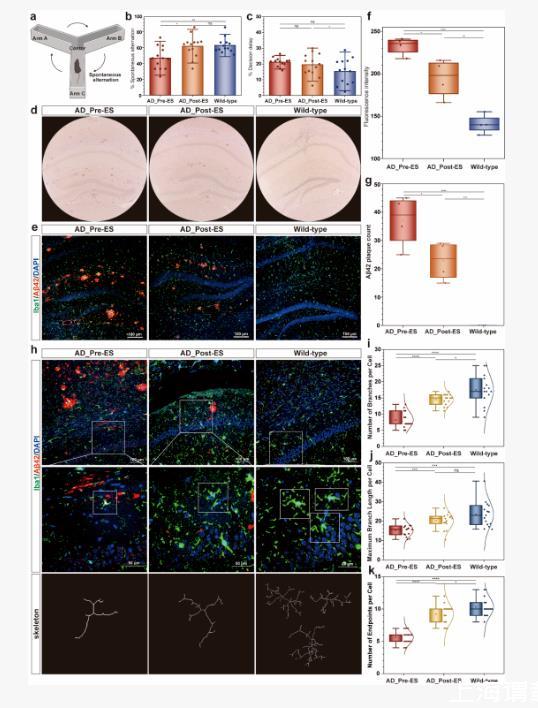
圖4.深腦靶向刺激改善阿爾茨海默模型小鼠認(rèn)知功能,減少Aβ42斑塊沉積
啟發(fā)與展望
本研究通過(guò)NeuroRevive-FlexChip首次在阿爾茨海默病模型小鼠中實(shí)現(xiàn)了對(duì)多巴胺釋放、電生理活動(dòng)與電刺激效應(yīng)的多模態(tài)協(xié)同檢測(cè)與調(diào)控,系統(tǒng)揭示了40Hz電刺激誘導(dǎo)的神經(jīng)環(huán)路功能重塑機(jī)制。研究發(fā)現(xiàn),AD模型小鼠存在異常高頻放電與多巴胺水平下調(diào),40Hz刺激能夠有效提升多巴胺釋放、抑制異常同步放電,并伴隨行為改善與Aβ42負(fù)荷下降,構(gòu)建了從神經(jīng)活動(dòng)、神經(jīng)遞質(zhì)調(diào)控到病理緩解的完整干預(yù)鏈條。此外,研究表明神經(jīng)元放電模式的變化與多巴胺濃度動(dòng)態(tài)呈高度耦合關(guān)系,提示刺激頻率與內(nèi)源性神經(jīng)節(jié)律可能存在功能共振,為理解AD中神經(jīng)調(diào)控節(jié)律失衡提供了新視角。該研究不僅驗(yàn)證了40Hz神經(jīng)調(diào)控的可行性與多層效應(yīng),也為多巴胺系統(tǒng)在AD中的作用提供了直接電化學(xué)證據(jù)。
本工作展示了柔性腦機(jī)接口神經(jīng)微電極在神經(jīng)退行性疾病研究中的巨大潛力,為實(shí)現(xiàn)精準(zhǔn)、實(shí)時(shí)、閉環(huán)的神經(jīng)調(diào)控提供了新范式。未來(lái)研究可基于此平臺(tái)拓展至多遞質(zhì)(如谷氨酸、GABA、5-HT)聯(lián)合檢測(cè),并集成多腦區(qū)同步采集與調(diào)控,解析更復(fù)雜的神經(jīng)調(diào)控網(wǎng)絡(luò)。
 相關(guān)新聞
相關(guān)新聞