熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
結果與討論
N?O生成特性
經過4個月以上運行期,A?-SBR和AO-SBR實現穩定的脫氮除磷。批次實驗1考察反硝化除磷與傳統反硝化過程N?O生成的差異。
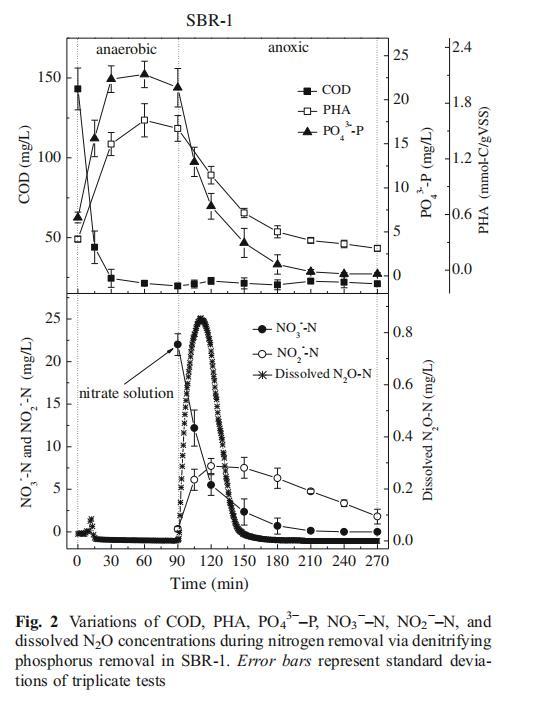
圖2和圖3展示典型周期內反硝化除磷(SBR-1)與傳統反硝化(SBR-2)過程中COD、氮、磷和PHA的變化。SBR-1厭氧階段,COD在30分鐘內迅速降至最低,伴隨PHA合成和PO?3?-P釋放。后續缺氧階段發生同步反硝化與PO?3?-P攝取,PHA被消耗(圖2),呈現典型DPAOs表型。SBR-2僅含缺氧階段,期間COD消耗、NO??-N還原和PO?3?-P釋放同時發生,僅生成少量PHA(圖3),呈現傳統反硝化菌表型。
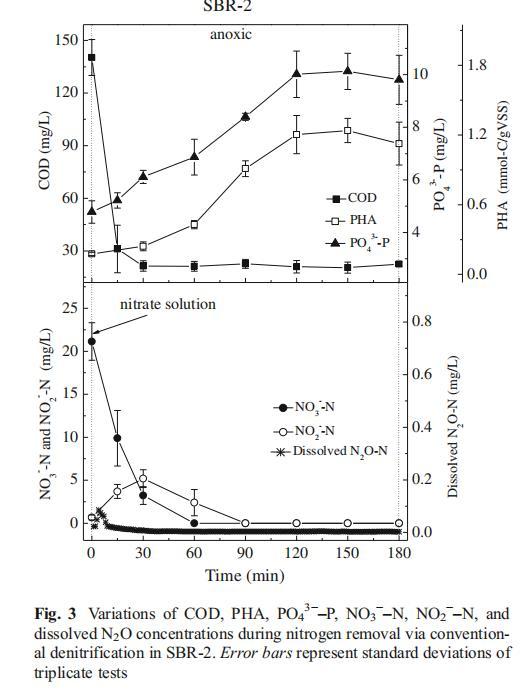
SBR-1中,N?O主要在缺氧階段生成,厭氧階段幾乎未檢測到;KNO?溶液投加后,溶解態N?O-N濃度在前15分鐘迅速升至0.87 mg/L,隨后急劇降至接近零(圖2)。類似地,SBR-2缺氧初期也觀察到N?O瞬時積累(圖3),但其最高溶解態N?O濃度僅0.08 mg/L,遠低于SBR-1。此外,尾氣N?O也被測定,氣相和液相總N?O生成量見表1。可見SBR-1的N?O生成量(占TN去除量的0.41±0.034%)雖顯著高于SBR-2(0.013±0.0056%),但遠低于先前反硝化除磷系統的報道值(2.34–21.6%)(Wang et al.2011a,b)。這可能歸因于使用了丙酸鹽與乙酸鹽的混合碳源,而非單一乙酸鹽。相較于乙酸鹽,丙酸鹽作為碳源顯著降低了廢水處理過程的N?O生成(Zhu and Chen 2011)。
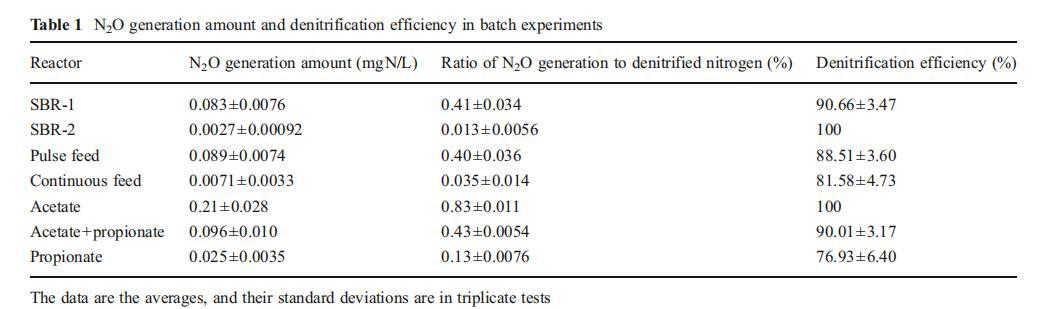
表1批次實驗中N?O生成量與反硝化效率
識別反硝化除磷中一氧化二氮生成的成因
SBR-1使用PHA作為反硝化碳源,SBR-2使用乙酸鹽和丙酸鹽。因此推測,使用PHA進行反硝化及高NO??-N積累是導致兩反應器N?O生成差異的原因。
使用PHA反硝化導致N?O生成
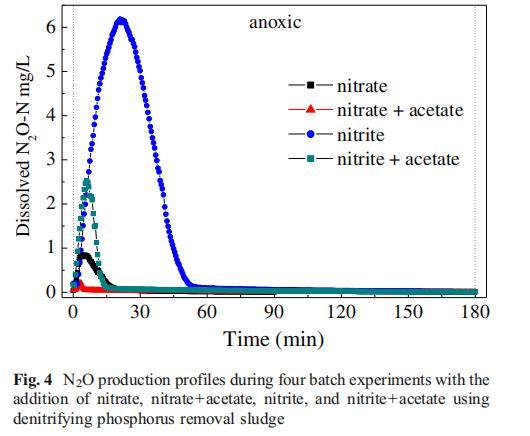
該成因首先通過向反硝化除磷污泥的缺氧批次實驗2中添加乙酸鹽驗證(圖4)。結果顯示:未添加乙酸鹽時,DPAOs利用厭氧階段合成的PHA作為反硝化碳源,最大N?O-N積累量達0.85 mg/L;添加乙酸鹽后,DPAOs可利用乙酸鹽作為反硝化碳源,最大N?O-N積累量僅0.21 mg/L。這表明使用PHA反硝化會增加N?O生成。相較于乙酸鹽,PHA降解速率較慢,無法為反硝化提供充足電子,導致反硝化酶之間競爭電子(Kampschreur et al.2009)。N?O還原酶(Nos)因還原N?O是反硝化最后一步而缺乏競爭優勢,抑制了N?O還原(Kampschreur et al.2009;Wang et al.2011b)。
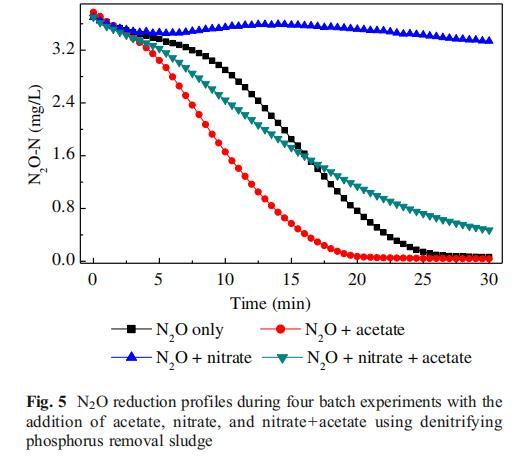
為驗證該假設,進行批次實驗3,結果如圖5所示。乙酸鹽添加顯著提高了N?O還原速率,因乙酸鹽降解速率是PHA的6–20倍,Nos可獲得充足電子還原N?O(Third et al.2003)。當添加硝酸鹽時,硝酸鹽還原酶(Nar)在電子競爭中優于Nos,PHA氧化提供的電子優先用于硝酸鹽還原,抑制了N?O還原(Kampschreur et al.2009)。而同時供應乙酸鹽和硝酸鹽時,乙酸鹽提供的電子足以支持硝酸鹽和N?O的還原,故N?O還原不受抑制。這些結果表明,使用PHA反硝化時,有限的電子無法滿足反硝化酶需求,且Nos與Nar競爭電子的能力較弱。
高NO??-N濃度導致N?O生成
圖2和圖3顯示,SBR-1的NO??-N積累高達8.51 mg/L,遠高于SBR-2(4.91 mg/L)。可能原因是SBR-1使用內碳源(PHA)反硝化,而SBR-2使用乙酸和丙酸。較低的PHA降解速率導致反硝化酶競爭電子,硝酸鹽還原速率遠高于亞硝酸鹽還原速率(Kampschreur et al.2009;Wang et al.2011b)。批次實驗2進一步證實NO??-N積累導致N?O生成。
圖4顯示,向DPAOs污泥添加亞硝酸鹽顯著刺激N?O生成,最大N?O-N積累量達6.19 mg/L,遠高于硝酸鹽添加反應器。該結果與Lemaire et al.(2006)一致,表明亞硝酸鹽添加的N?O生成速率是硝酸鹽的五倍。類似地,Zhou et al.(2008a)證實高濃度NO??-N導致N?O積累,其后續研究揭示Nos活性受高NO??-N積累抑制(Zhou et al.2011)。
但批次實驗2發現有趣現象(圖4):當同時添加亞硝酸鹽和乙酸鹽時,N?O生成遠低于僅添加亞硝酸鹽的反應器。這解釋了為何傳統反硝化過程盡管NO??-N積累達4.91 mg/L,卻幾乎不產生N?O——外碳源可減輕亞硝酸鹽對Nos活性的抑制。
綜上,Nos競爭電子的弱勢和高NO??-N積累是反硝化除磷系統N?O生成的兩大主因。
控制反硝化除磷過程中的一氧化二氮生成
反硝化除磷利用同一碳源同步脫氮除磷,具有節約碳源和氧氣的巨大潛力。但大量N?O生成嚴重阻礙其應用。基于上述分析,可通過兩種途徑降低N?O生成:(a)連續投加硝酸鹽以減少反硝化酶間電子競爭;(b)使用丙酸鹽作為碳源以減少亞硝酸鹽積累。
硝酸鹽投加策略對一氧化二氮生成的影響
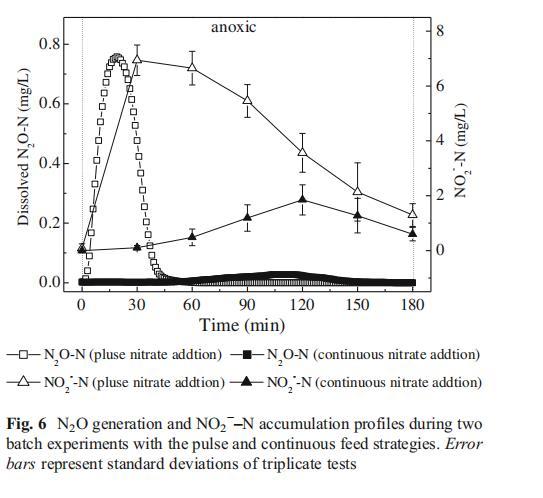
硝酸鹽脈沖投加時,缺氧階段初始NO??-N濃度始終較高(25 mg/L)。PHA氧化提供的電子不足以將NO??完全還原為N?,有限的電子優先用于將NO??-N還原為NO??-N和N?O。若采用連續投加策略,NO??-N濃度可維持在較低水平。此時,NO??-N完全還原為N?的電子需求可被滿足,從而減少N?O積累。通過批次實驗4比較脈沖與連續投加條件下的N?O和NO??-N積累。圖6顯示兩種策略下N?O生成差異:連續投加顯著降低N?O生成和NO??-N積累。Zhou et al.(2008b)同樣發現,通過連續向缺氧階段輸送含亞硝酸鹽的液流,新型兩污泥三級系統的N?O生成減少。
碳源對一氧化二氮生成的影響
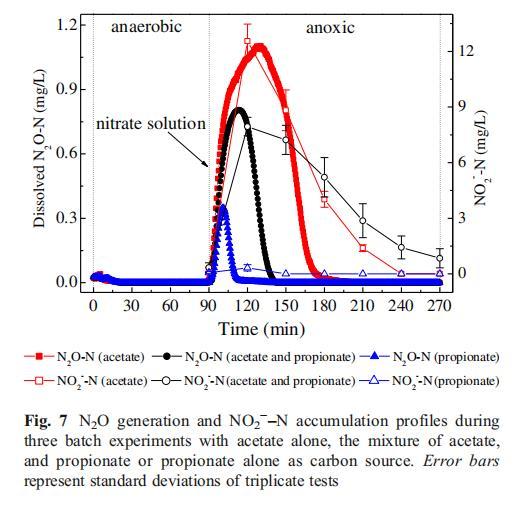
NO??-N積累是反硝化除磷中N?O生成的主因。若減少NO??-N積累,則可降低N?O生成。丙酸鹽是DPAOs的良好碳源,可減少反硝化除磷過程中的NO??-N積累(Carvalho et al.2007)。因此,以丙酸鹽為DPAOs碳源可減少N?O生成。批次實驗5結果清晰證實丙酸鹽的減排優勢(圖7,表1):相較于乙酸鹽及乙丙混合酸鹽,單獨使用丙酸鹽顯著降低NO??-N積累和N?O生成。NO??-N是反硝化中間產物,其積累受硝酸鹽還原酶(Nar)和亞硝酸鹽還原酶(Nir)活性影響(Wang et al.2011a)。碳源對Nar和Nir活性有不同影響,導致硝酸鹽還原速率(N1)與亞硝酸鹽還原速率(N2)比值不同。高N1/N2比會導致高NO??-N積累(Wang et al.2011a;Zhu and Chen 2011)。如表2所示,丙酸鹽降低了N1/N2比,與較低的NO??-N積累一致。
表2不同碳源下NO??-N與NO??-N還原速率比較
*數據為三次測試的平均值±標準偏差
但該結果與Wang et al.(2011a)結論相悖,其短期實驗發現使用乙丙混合酸鹽或丙酸鹽時N?O生成顯著增加。差異在于本研究DPAOs由乙丙混合酸鹽馴化,而該研究僅用乙酸鹽馴化。兩研究的DPAOs種類可能不同,需進一步探究不同碳源馴化的反硝化除磷系統中N?O生成與微生物群落的關系。
因此,連續投加硝酸鹽或使用丙酸鹽為碳源均可減少反硝化除磷過程的N?O生成。此外,減少厭氧時間、使用污泥堿性發酵液及添加銅離子(Cu2?)等措施也有報道可降低生物脫氮除磷過程的N?O生成(Wang et al.2011b;Zhu and Chen 2011;Zhu et al.2012),其在反硝化除磷工藝中的適用性值得深入研究。
結論
相較于傳統反硝化過程,反硝化除磷過程顯著增加N?O生成。兩大主因導致此現象:一是利用PHA反硝化引發反硝化酶間電子競爭,N?O還原酶在電子捕獲中缺乏競爭優勢;二是過量亞硝酸鹽積累抑制N?O還原酶活性。因此,可通過兩種途徑降低N?O生成:(a)連續投加硝酸鹽減少反硝化酶間電子競爭;(b)使用丙酸鹽為碳源減少亞硝酸鹽積累。
 相關新聞
相關新聞