熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
Synergy of hypoxia relief and chromatin remodeling to overcome tumor radiation resistance
緩解缺氧和染色質(zhì)重塑的協(xié)同作用,以克服腫瘤輻射抵抗
來源:Biomaterials Science Published on 23 July 2020.
1. 論文摘要核心內(nèi)容
研究開發(fā)了一種多功能納米顆粒 CAT-SAHA@PLGA:
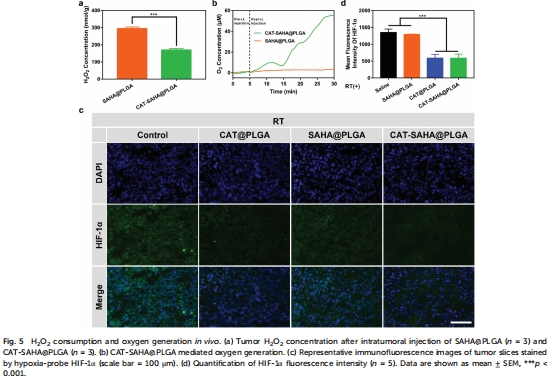
過氧化氫酶(CAT) 分解腫瘤內(nèi)過氧化氫(H?O?)產(chǎn)生氧氣,緩解腫瘤缺氧(圖5b)。
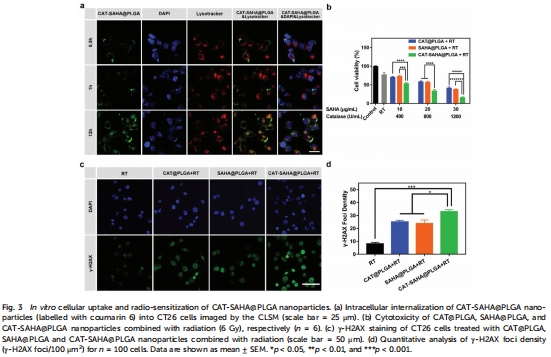
組蛋白去乙酰化酶抑制劑(SAHA) 松弛染色質(zhì)結(jié)構(gòu),增強(qiáng)DNA對(duì)放療的敏感性(圖3c-d)。
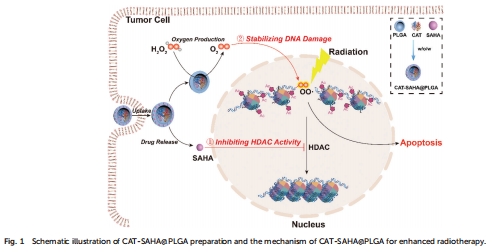
雙重協(xié)同機(jī)制:
缺氧緩解提升放療產(chǎn)生的活性氧(ROS)穩(wěn)定性。
染色質(zhì)重塑使DNA更易受氧化損傷(圖1)。
療效:在結(jié)腸癌(CT26)模型中,聯(lián)合放療使腫瘤抑制率達(dá) 87.28%(圖6b),顯著優(yōu)于單藥治療。

2. 研究目的
解決腫瘤微環(huán)境中 缺氧 和 HDAC過表達(dá) 導(dǎo)致的放療抵抗,通過納米載體共遞送CAT與SAHA,實(shí)現(xiàn)放療增敏。
3. 研究思路
1.納米顆粒設(shè)計(jì):
采用 水/油/水雙乳化法 制備PLGA納米顆粒,將親水性CAT封裝在內(nèi)腔,疏水性SAHA嵌入PLGA外殼(圖1)。
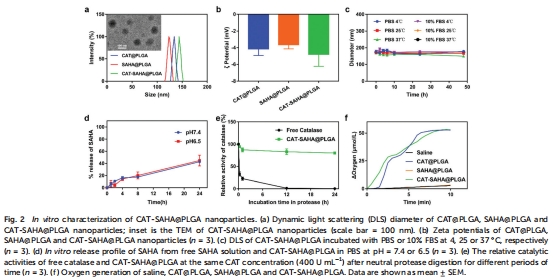
粒徑約144 nm(圖2a),Zeta電位-4.80 mV(圖2b),穩(wěn)定性良好(48小時(shí)內(nèi)粒徑無顯著變化,圖2c)。
2.機(jī)制驗(yàn)證:
缺氧緩解:CAT分解H?O?產(chǎn)氧,Unisense電極實(shí)時(shí)監(jiān)測(cè)瘤內(nèi)氧濃度升至55 μM(圖5b)。
染色質(zhì)重塑:SAHA抑制HDAC,增加組蛋白乙酰化,γ-H2AX染色顯示DNA損傷增強(qiáng)(圖3c-d)。
3.體內(nèi)外評(píng)價(jià):
體外:聯(lián)合放療使CT26細(xì)胞存活率降低至20%(圖3b)。
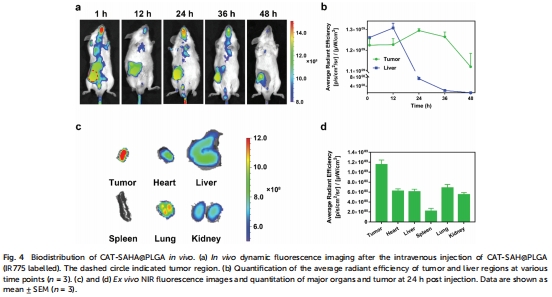
體內(nèi):靜脈注射后納米顆粒在腫瘤富集(圖4b),聯(lián)合放療顯著抑制腫瘤生長(圖6a-b)。
4. 關(guān)鍵數(shù)據(jù)及研究意義
(1) 納米顆粒特性與藥物釋放(圖2)
數(shù)據(jù):
包封率:CAT 66.88%,SAHA 18.78%(表S1-S2)。
SAHA緩釋:24小時(shí)釋放40%(圖2d)。
CAT活性保護(hù):蛋白酶環(huán)境中保持80%活性(圖2e)。
意義:PLGA外殼有效保護(hù)CAT活性,延長SAHA循環(huán)時(shí)間,解決裸酶易降解和HDAC抑制劑藥代動(dòng)力學(xué)差的問題。
(2) 缺氧緩解與氧動(dòng)力學(xué)(圖5)
數(shù)據(jù):
CAT-SAHA@PLGA注射后,瘤內(nèi)H?O?濃度下降50%(圖5a),氧濃度瞬時(shí)升至55 μM(圖5b)。
HIF-1α表達(dá)顯著降低(圖5d),證實(shí)缺氧逆轉(zhuǎn)。
意義:直接驗(yàn)證CAT的催化活性在體內(nèi)有效,為放療增敏提供氧支持。
(3) 放療增敏機(jī)制(圖3 & 圖6)
數(shù)據(jù):
DNA損傷:γ-H2AX焦點(diǎn)密度增加3倍(圖3d),表明DNA雙鏈斷裂加劇。
體內(nèi)療效:聯(lián)合放療組腫瘤體積縮小87.28%(圖6b),Ki67增殖標(biāo)志物減少,TUNEL凋亡增加(圖6d-f)。
意義:協(xié)同機(jī)制顯著提升放療療效,SAHA松弛染色質(zhì)使DNA更易受氧自由基損傷。
5. 結(jié)論
1.協(xié)同增敏:CAT緩解缺氧 + SAHA重塑染色質(zhì),克服單一策略的局限性。
2.納米載體優(yōu)勢(shì):PLGA納米顆粒保護(hù)CAT活性,延長SAHA半衰期(t?/?從2.6小時(shí)增至3.95小時(shí)),提升腫瘤靶向性。
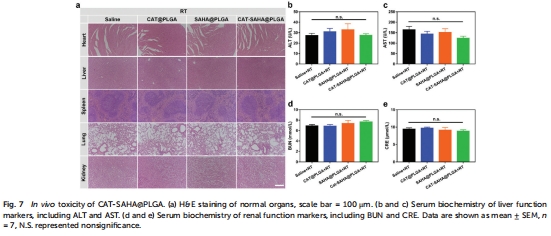
3.安全性:未觀察到顯著肝腎毒性或體重下降(圖7)。
6. 丹麥Unisense電極的核心價(jià)值
(1) 技術(shù)角色
實(shí)時(shí)動(dòng)態(tài)監(jiān)測(cè)瘤內(nèi)氧分壓:
使用Clark氧電極(OX25,Unisense)直接插入腫瘤組織,記錄注射納米顆粒后的氧濃度變化(方法4.8)。
關(guān)鍵數(shù)據(jù):注射CAT-SAHA@PLGA后,氧濃度在25分鐘內(nèi)從基線升至55 μM(圖5b)。
(2) 研究意義
機(jī)制驗(yàn)證:
直觀證明CAT在瘤內(nèi)的持續(xù)催化活性(H?O?→O?),推翻“裸酶在體內(nèi)易失活”的固有認(rèn)知。
揭示氧動(dòng)力學(xué)特征:產(chǎn)氧速率與持續(xù)時(shí)間,為放療時(shí)機(jī)選擇提供依據(jù)(如氧濃度>40 μM時(shí)放療效果最佳)。
方法學(xué)創(chuàng)新:
突破傳統(tǒng)終點(diǎn)法檢測(cè)(如HIF-1α染色)的局限,實(shí)現(xiàn) 原位、實(shí)時(shí)、定量 的氧監(jiān)測(cè)。
首次在體內(nèi)量化納米催化劑的瞬時(shí)氧生成能力,為類似研究提供金標(biāo)準(zhǔn)。
(3) 科學(xué)價(jià)值
療效關(guān)聯(lián)性:氧濃度峰值(55 μM)與放療抑制率(87.28%)直接關(guān)聯(lián),證實(shí)“缺氧緩解”是增敏的關(guān)鍵環(huán)節(jié)。
轉(zhuǎn)化啟示:Unisense電極的高靈敏度(μM級(jí)分辨率)適用于臨床腫瘤氧分壓監(jiān)測(cè),指導(dǎo)個(gè)體化放療方案。
總結(jié)
本研究通過 CAT產(chǎn)氧 + SAHA染色質(zhì)重塑 的協(xié)同策略,顯著提升放療療效。丹麥Unisense電極在 原位氧動(dòng)力學(xué)監(jiān)測(cè) 中發(fā)揮不可替代的作用:其微創(chuàng)針式探針直接量化瘤內(nèi)氧分壓變化,不僅驗(yàn)證了CAT的持續(xù)催化活性,更為“缺氧緩解增敏放療”的理論提供了最直接的實(shí)驗(yàn)證據(jù)。未來可基于此技術(shù)優(yōu)化放療時(shí)機(jī),實(shí)現(xiàn)氧濃度導(dǎo)向的精準(zhǔn)治療。