熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Carbonic anhydrase inhibitors suppress seizures in a rat model of birth asphyxia
碳酸酐酶抑制劑抑制出生窒息大鼠模型的癲癇發作
來源:Epilepsia. 2021;62:1971–1984.
1. 摘要核心內容
本研究證實碳酸酐酶抑制劑(CAIs)(乙酰唑胺AZA、苯唑胺BZA、依索唑胺EZA)通過誘導系統性呼吸性酸中毒,顯著抑制大鼠出生窒息模型中的癲癇發作:
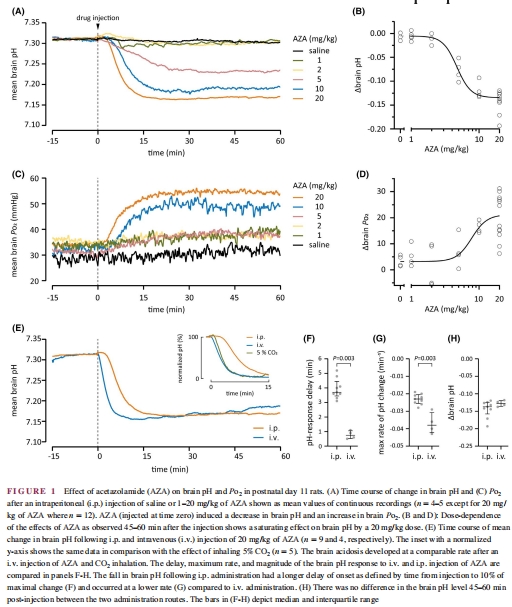
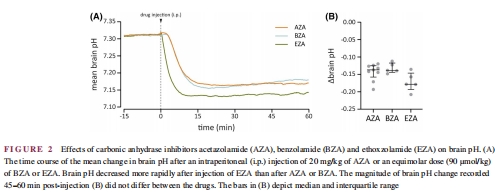
核心機制:CAIs抑制血管和血液中的碳酸酐酶,減緩CO?清除→升高血PCO?→腦pH降低0.14-0.17單位(圖1B, 2B),從而抑制神經元興奮性。
癲癇抑制效果:
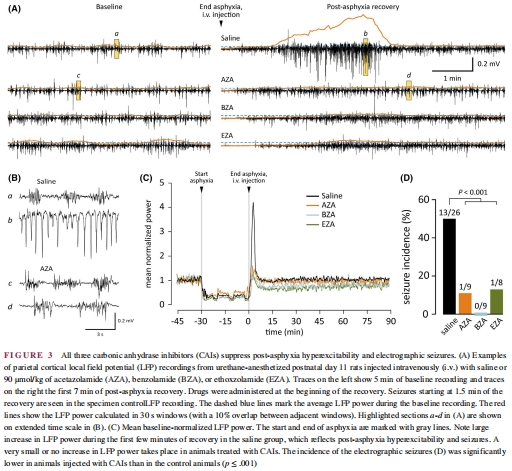
電生理記錄顯示,CAIs將窒息后癲癇發生率從50%降至<10%(圖3D)。
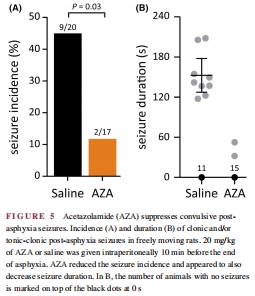
自由活動大鼠中,AZA將驚厥性癲癇發生率從45%降至12%(圖5A)。
安全性:AZA在新生兒中應用歷史悠久,可安全轉化為臨床輔助治療。
2. 研究目的
驗證CAIs能否通過延緩窒息后腦pH恢復(而非腦缺氧)抑制癲癇發作,并明確其作用機制是否依賴呼吸性酸中毒。
3. 研究思路
雙模型驗證→藥效對比→機制解析:
模型構建:
麻醉大鼠:11日齡大鼠暴露于間歇性窒息(3×[7 min 9% O? + 3 min 5% O?] + 20% CO?),實時監測腦pH、PO?及局部場電位(LFP)(圖1-4)。

自由活動大鼠:觀察窒息后行為性癲癇及血液酸堿參數(圖5-6)。
藥物干預:
窒息后立即靜脈注射CAIs(AZA/BZA/EZA,90 μmol/kg)。
對比不同脂溶性CAIs(EZA > AZA > BZA)的藥效動力學差異。
分析維度:
腦酸堿平衡:pH動態變化(圖1,2,4)、PO?(圖1,4)。
癲癇活動:LFP癲癇樣放電(圖3)、行為性驚厥(圖5)。
系統效應:血液PCO?、HCO??(圖6)。
4. 關鍵數據及研究意義
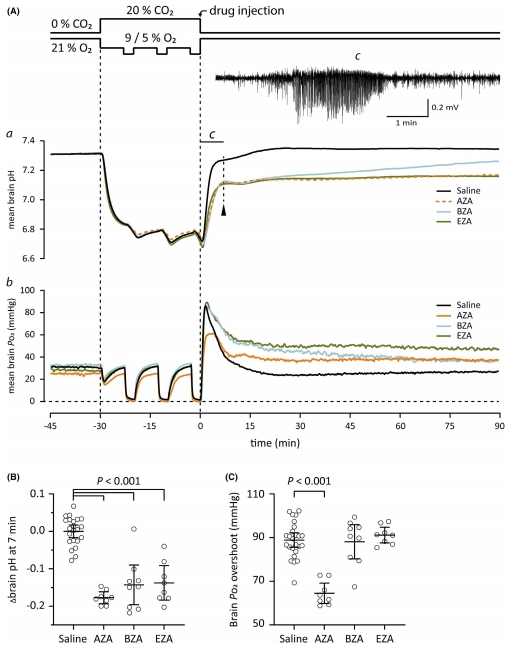
(1)CAIs誘導腦酸中毒(圖1,2)
數據:
20 mg/kg AZA腹腔注射使腦pH↓0.14單位(45-60 min)(圖1B)。
靜脈注射AZA/pH下降速度≈吸入5% CO?(圖1E),證實快速呼吸性酸中毒。
EZA起效最快(0.8 min),但三者最終酸中毒程度無差異(圖2)。
意義:CAIs通過抑制血管/血液碳酸酐酶(非腦內)誘導酸中毒,與脂溶性無關。
(2)癲癇抑制與pH恢復延緩(圖3,4)
數據:
對照組:50%大鼠出現LFP癲癇(潛伏期141 s),持續80 s(圖3D)。
CAIs組:癲癇發生率<10%(AZA/BZA/EZA均有效)(圖3D)。
腦pH恢復分兩階段:快速期(0-7 min)pH↑0.53單位,CAIs使其↓0.14-0.18單位(圖4B)。
意義:癲癇發生于腦pH快速恢復期,CAIs通過延緩pH恢復速率(非絕對pH值)阻斷癲癇。
(3)PO?變化與癲癇無關(圖4)
數據:
窒息后腦PO?迅速恢復并超調(89 mmHg),CAIs不改變此過程時程(圖4A,C)。
AZA降低PO?超調峰值(65 vs 89 mmHg),但癲癇抑制效果與其他CAIs無差異。
意義:CAIs抗癲癇作用依賴pH而非PO?變化。
(4)自由活動大鼠驗證(圖5)
數據:
AZA腹腔注射(窒息前10 min)使驚厥性癲癇發生率從9/20降至2/17(圖5A)。
癲癇持續時間從153 s縮短至<53 s。
意義:CAIs在清醒動物中仍有效,且給藥時機靈活。
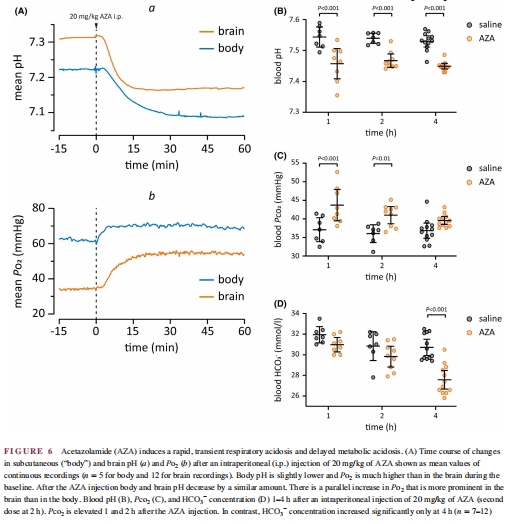
(5)呼吸性酸中毒主導機制(圖6)
數據:
AZA注射后2 h內:血PCO?↑(呼吸性酸中毒),HCO??不變(圖6B-D)。
4 h后:HCO??↓(代謝性酸中毒),但癲癇已終止。
意義:抗癲癇作用由早期呼吸性酸中毒介導,與后期代謝性酸中毒無關。
5. 核心結論
pH恢復速率觸發癲癇:窒息后腦pH快速恢復是癲癇發作的關鍵誘因(非缺氧本身)。
CAIs三重優勢:
快速誘導呼吸性酸中毒(腦pH↓0.14-0.17單位)。
高效抑制電生理及行為性癲癇(有效率>80%)。
不同脂溶性CAIs效果相當,提示作用靶點在血管/血液而非腦內。
臨床轉化潛力:AZA已用于新生兒青光眼/腦水腫,可安全復用于窒息后癲癇的輔助治療。
6. 丹麥Unisense電極的研究意義
技術應用與數據:
功能:使用Unisense pH-25和OX-10微電極實時監測腦組織pH和PO?(方法部分)。
關鍵發現:
捕捉窒息后腦pH快速恢復兩階段(圖4A):0-7 min↑0.53單位→后續緩慢恢復。
揭示CAIs給藥后腦pH↓0.14-0.17單位(圖1A, 2A),PO?↑16-21 mmHg(圖1C)。
證實pH變化速率與癲癇潛伏期負相關(圖3-4)。
科學價值:
高時空分辨率:
電極直徑25 μm(pH)和10 μm(PO?),實現皮層局部實時監測(秒級響應),避免終末采樣偏差。
揭示CAIs靜脈注射后1分鐘內腦pH即下降(圖1E),為快速起效提供直接證據。
機制解析關鍵工具:
明確癲癇發生于pH恢復期而非缺氧期(PO?在癲癇前已恢復正常)(圖4)。
區分酸中毒類型:呼吸性(PCO?↑)主導早期抗癲癇作用(圖6)。
藥效動力學標尺:
量化不同CAIs的起效時間(EZA: 0.8 min vs AZA: 3.7 min)(圖2A),指導臨床給藥方式選擇。
領域貢獻:
為pH調控抗癲癇理論提供精準實驗支持,推動靶向碳酸酐酶的神經保護策略。
確立Unisense電極為腦酸堿/氧代謝研究的金標準工具。