熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
Hydrogen Sulfide Is a Regulator of Hemoglobin Oxygen-Carrying Capacity via Controlling 2,3-BPG Production in Erythrocytes
硫化氫通過(guò)控制紅細(xì)胞中 2,3-BPG 的產(chǎn)生來(lái)調(diào)節(jié)血紅蛋白攜氧能力
來(lái)源:Oxidative Medicine and Cellular Longevity Volume 2021, Article ID 8877691, 16 pages
1. 摘要核心內(nèi)容
本研究首次揭示內(nèi)源性硫化氫(H?S) 是紅細(xì)胞內(nèi) 2,3-二磷酸甘油酸(2,3-BPG) 產(chǎn)生的關(guān)鍵抑制因子,通過(guò)調(diào)節(jié)血紅蛋白(Hb)與細(xì)胞膜的錨定狀態(tài),控制雙磷酸甘油酸變位酶(BPGM)的亞細(xì)胞定位,從而影響Hb-O?結(jié)合親和力。主要發(fā)現(xiàn):
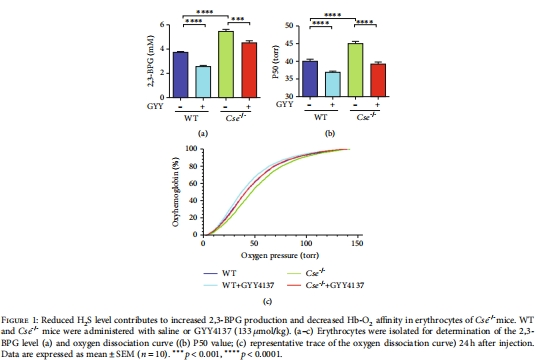
H?S缺失導(dǎo)致2,3-BPG升高:胱硫醚-γ-裂解酶(CSE)基因敲除(Cse?/?)小鼠紅細(xì)胞中2,3-BPG水平顯著增加,50%氧飽和度(P50)值升高(圖1a-c)。
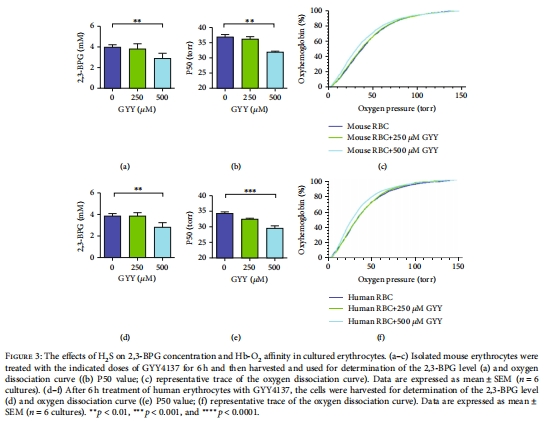
H?S直接作用于紅細(xì)胞:體外實(shí)驗(yàn)證實(shí)H?S供體GYY4137可降低2,3-BPG并增強(qiáng)Hb-O?親和力(圖3)。
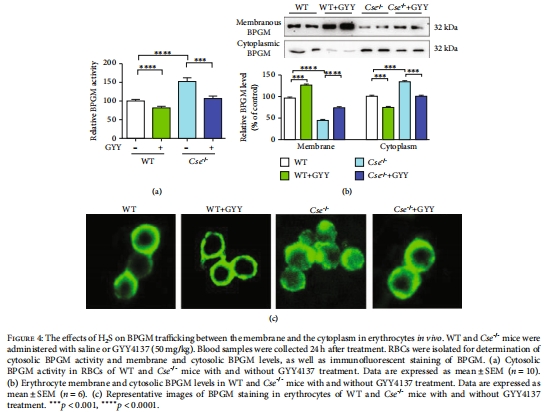
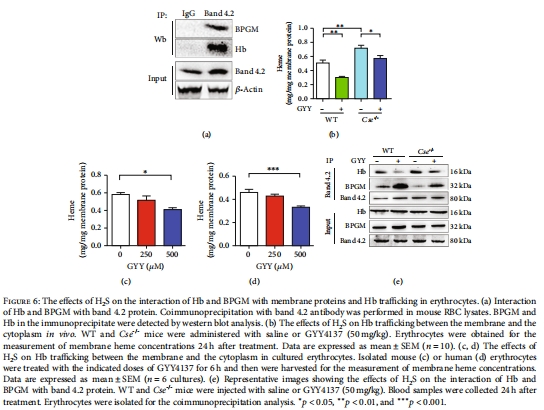
分子機(jī)制:H?S通過(guò)促進(jìn)Hb從膜釋放至胞質(zhì),增強(qiáng)BPGM膜錨定(圖4-6),該過(guò)程與Hb的S-硫磺化修飾(Cys104位點(diǎn))相關(guān)(圖7)。
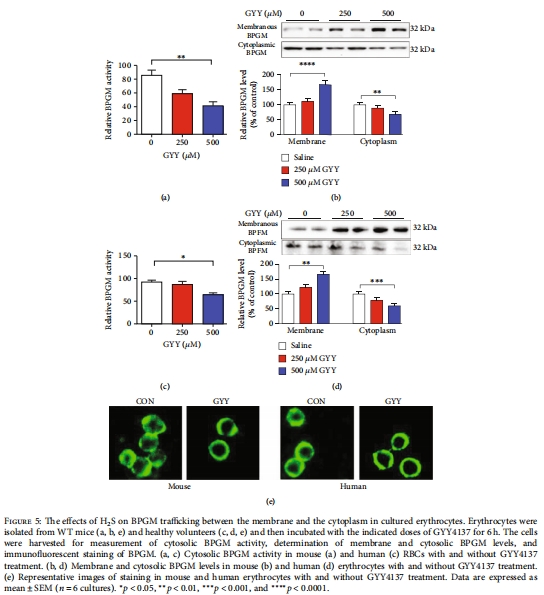
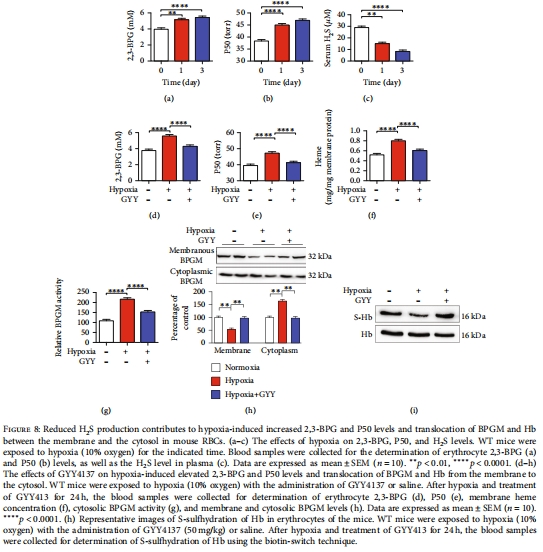
缺氧適應(yīng)性:缺氧降低循環(huán)H?S水平,增加2,3-BPG,而GYY4137可逆轉(zhuǎn)此效應(yīng)(圖8)。
2. 研究目的
探究H?S是否及如何調(diào)節(jié)紅細(xì)胞內(nèi)2,3-BPG代謝和Hb-O?親和力,特別是在缺氧適應(yīng)中的作用,為紅細(xì)胞氧運(yùn)輸調(diào)控提供新機(jī)制。
3. 研究思路
基因模型→代謝組學(xué)→機(jī)制解析→缺氧驗(yàn)證:
動(dòng)物模型:
比較Cse?/?小鼠與野生型(WT)紅細(xì)胞代謝差異(代謝組學(xué)分析,圖1)。
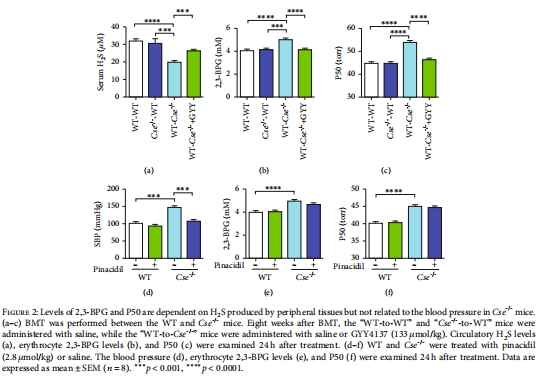
骨髓移植實(shí)驗(yàn)區(qū)分H?S來(lái)源(外周組織 vs. 紅細(xì)胞自身,圖2)。
體外驗(yàn)證:
人/鼠紅細(xì)胞培養(yǎng)體系,添加H?S供體(GYY4137)或抑制劑(碘乙酰胺)。
檢測(cè)2,3-BPG、P50、BPGM亞細(xì)胞定位(圖3-5)。
分子機(jī)制:
免疫共沉淀(Co-IP)和質(zhì)譜分析Hb與BPGM的相互作用(圖6)。
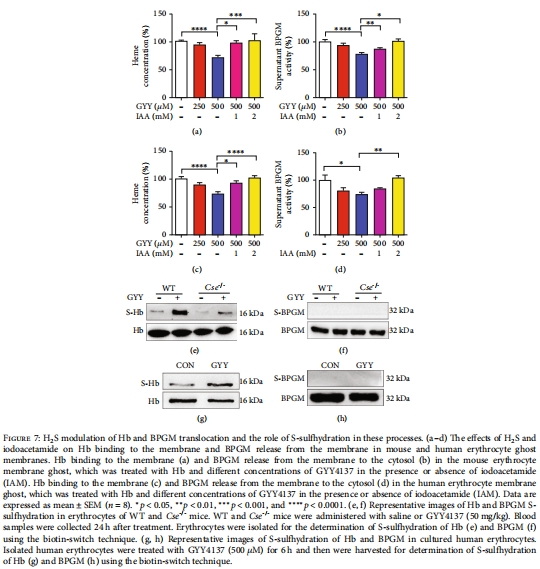
S-硫磺化修飾檢測(cè)(生物素轉(zhuǎn)換法,圖7)。
缺氧模型:
10% O?處理小鼠,監(jiān)測(cè)H?S水平與2,3-BPG動(dòng)態(tài)變化(圖8)。
4. 關(guān)鍵數(shù)據(jù)及研究意義
(1)H?S缺失增加2,3-BPG與P50(圖1)
數(shù)據(jù):Cse?/?小鼠紅細(xì)胞2,3-BPG升高40%,P50增加4-6 mmHg(圖1a-c)。
意義:首次證明內(nèi)源性H?S是2,3-BPG的生理性抑制因子,維持正常Hb-O?親和力。
(2)H?S調(diào)控BPGM膜-胞質(zhì)轉(zhuǎn)運(yùn)(圖4-5)
數(shù)據(jù):
Cse?/?小鼠胞質(zhì)BPGM活性升高2倍,膜錨定BPGM減少(圖4a-b)。
GYY4137處理逆轉(zhuǎn)BPGM膜定位(免疫熒光,圖4c)。
意義:揭示H?S通過(guò)控制BPGM亞細(xì)胞分布調(diào)節(jié)2,3-BPG合成,突破傳統(tǒng)代謝酶活性調(diào)控認(rèn)知。
(3)Hb S-硫磺化修飾的關(guān)鍵作用(圖7)
數(shù)據(jù):
MS鑒定Hb α鏈Cys104為S-硫磺化位點(diǎn)(圖7e-g)。
H?S缺失降低修飾水平,增加Hb膜錨定(膜血紅素含量升高,圖6b-d)。
意義:提出 H?S-Hb-BPGM軸新機(jī)制——S-硫磺化促進(jìn)Hb胞質(zhì)游離,減少與BPGM競(jìng)爭(zhēng)性膜結(jié)合。
(4)缺氧通過(guò)H?S下調(diào)適應(yīng)氧運(yùn)輸(圖8)
數(shù)據(jù):缺氧24小時(shí),循環(huán)H?S下降50%,2,3-BPG升高35%,P50增加15%(圖8a-c)。
意義:闡明缺氧適應(yīng)性新通路——低H?S→高2,3-BPG→Hb氧親和力降低→優(yōu)化組織氧釋放。
5. 核心結(jié)論
H?S是紅細(xì)胞氧親和力核心調(diào)節(jié)因子:通過(guò)抑制2,3-BPG合成維持正常Hb-O?結(jié)合。
分子機(jī)制依賴Hb-BPGM空間競(jìng)爭(zhēng):H?S通過(guò)S-硫磺化修飾(Cys104)促進(jìn)Hb胞質(zhì)游離,增強(qiáng)BPGM膜錨定,抑制2,3-BPG生成。
缺氧適應(yīng)性關(guān)鍵環(huán)節(jié):缺氧降低H?S水平,解除對(duì)2,3-BPG的抑制,提升氧釋放能力。
轉(zhuǎn)化潛力:H?S供體(如GYY4137)可干預(yù)缺氧相關(guān)病理狀態(tài)。
6. 丹麥Unisense電極的研究意義
技術(shù)原理與優(yōu)勢(shì):
微呼吸傳感器(H?S-MRCh):實(shí)時(shí)監(jiān)測(cè)H?S生成動(dòng)力學(xué)(方法2.11)。
高靈敏度與實(shí)時(shí)性:檢測(cè)限達(dá)微摩爾級(jí),動(dòng)態(tài)追蹤H?S生成速率(圖S2)。
關(guān)鍵科學(xué)貢獻(xiàn):
量化紅細(xì)胞H?S生成能力:
直接證實(shí)小鼠紅細(xì)胞存在CSE依賴性H?S合成(Cse?/?小鼠生成率降低60%,圖S2)。
發(fā)現(xiàn)人紅細(xì)胞H?S生成速率與2,3-BPG負(fù)相關(guān)(圖3d-f)。
揭示缺氧對(duì)H?S代謝的即時(shí)影響:
Unisense動(dòng)態(tài)曲線顯示:缺氧1小時(shí)內(nèi)H?S生成速率下降40%,為"缺氧→H?S↓→2,3-BPG↑"鏈條提供時(shí)間分辨證據(jù)(圖8c)。
解析H?S供體藥效動(dòng)力學(xué):
GYY4137處理后H?S生成速率緩升,持續(xù)>6小時(shí)(圖3a),解釋其長(zhǎng)效調(diào)控2,3-BPG的機(jī)制。
領(lǐng)域突破性價(jià)值:
克服傳統(tǒng)終點(diǎn)法(亞甲基藍(lán)法)的低通量局限,實(shí)現(xiàn)活細(xì)胞H?S代謝實(shí)時(shí)監(jiān)測(cè);
為氣體信號(hào)分子研究提供動(dòng)態(tài)量化工具,推動(dòng)紅細(xì)胞代謝調(diào)控向?qū)崟r(shí)化、精準(zhǔn)化發(fā)展。