熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
Methylmercury formation in boreal wetlands in relation to chemical speciation of mercury(II) and concentration of low molecular mass thiols
北方濕地中甲基汞的形成與汞的化學(xué)形態(tài)(II)和低分子量硫醇濃度的關(guān)系
來源:Science of the Total Environment 755 (2021) 142666
一、摘要概述
本研究探討了北方濕地土壤中甲基汞(MeHg)的形成機(jī)制,重點(diǎn)關(guān)注 汞(II)的化學(xué)形態(tài) 和 低分子量硫醇(LMM-RSH)濃度 的影響。關(guān)鍵發(fā)現(xiàn)包括:
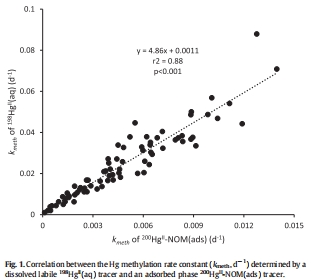
汞溶解度主導(dǎo)甲基化:孔隙水中溶解態(tài)汞(Hg(II)?q)的濃度是控制甲基化速率(k??)的關(guān)鍵因素,其甲基化潛力比吸附態(tài)汞(HgII-NOM(ads))高5倍(圖1)。
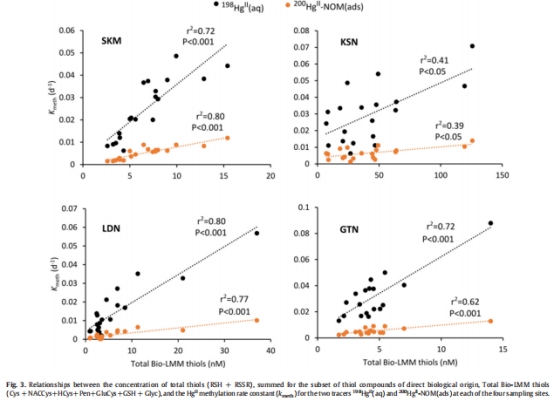
硫醇與甲基化正相關(guān):特定生物源低分子量硫醇(如半胱氨酸、谷胱甘肽)的濃度與k??顯著正相關(guān)(圖3),暗示微生物活動(dòng)驅(qū)動(dòng)甲基化。
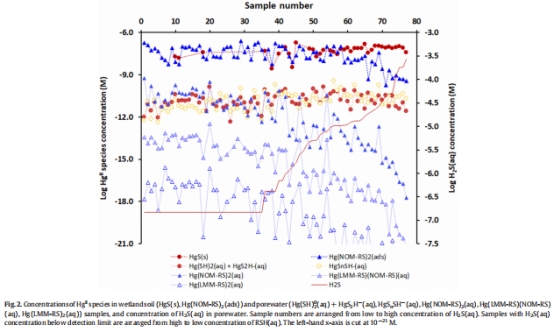
熱力學(xué)模型的局限性:盡管建立了全面的汞形態(tài)熱力學(xué)模型(涵蓋Hg2?與硫化物、多硫化物、有機(jī)硫醇的絡(luò)合),但模型未能預(yù)測(cè)k??(圖2)。
二、研究目的
解析汞生物可利用性:驗(yàn)證汞在固/吸附相的溶解度是否控制甲基化潛力。
評(píng)估形態(tài)模型預(yù)測(cè)能力:探究熱力學(xué)模型能否通過汞(II)的化學(xué)形態(tài)預(yù)測(cè)k??。
揭示硫醇的作用機(jī)制:明確低分子量硫醇(LMM-RSH)是否直接或間接調(diào)控MeHg形成。
三、研究思路
采用 “多場(chǎng)地采樣→雙同位素示蹤→多組學(xué)分析” 策略:
樣本采集:在瑞典北部(SKM、KSN)和南部(LDN、GTN)的4個(gè)北方濕地采集77個(gè)土壤和孔隙水樣本(5 cm深度間隔,0–25 cm)。
同位素示蹤:
高生物可利用性示蹤劑:1??Hg(OH)?(aq)(溶解態(tài)汞)。
低生物可利用性示蹤劑:2??HgII-NOM(ads)(吸附于有機(jī)質(zhì)的汞)。
甲基化潛力測(cè)定:通過48小時(shí)厭氧培養(yǎng)測(cè)定k??(甲基化速率常數(shù))。
多參數(shù)分析:
汞形態(tài):熱力學(xué)模型計(jì)算孔隙水中Hg2?的絡(luò)合物(硫化物、多硫化物、NOM/LMM硫醇)。
硫醇濃度:LC-ESI-MS定量10種LMM-RSH(如半胱氨酸、谷胱甘肽)。
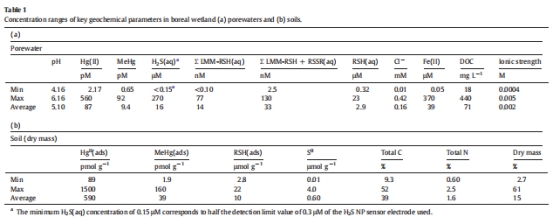
輔助參數(shù):pH、H?S、DOC、Fe(II)等(表1)。
四、關(guān)鍵數(shù)據(jù)及研究意義
1. 甲基化潛力(k??)差異(圖1)
數(shù)據(jù)來源:雙同位素示蹤實(shí)驗(yàn)(1??Hg(aq) vs. 2??Hg-NOM(ads))。
結(jié)果:1??Hg(aq)的k??平均比2??Hg-NOM(ads)高5倍(R2=0.88)。
意義:證實(shí) 汞溶解度(而非化學(xué)形態(tài))是甲基化的主要限制因素,吸附態(tài)汞的解吸動(dòng)力學(xué)限制了生物可利用性。
2. 汞化學(xué)形態(tài)分布(圖2)
數(shù)據(jù)來源:熱力學(xué)模型計(jì)算孔隙水中Hg2?的形態(tài)(Hg(SH)?、HgS?SH?、Hg(NOM-RS)?等)。
結(jié)果:Hg(NOM-RS)?(aq)和Hg(多硫化物)占主導(dǎo),LMM-RSH絡(luò)合物(如Hg(半胱氨酸)?)濃度極低(平均<0.000038 pM)。
意義:盡管形態(tài)分布廣泛(硫醇主導(dǎo)→硫化物主導(dǎo)),但形態(tài)與k??無顯著相關(guān)性(R2=0.14),挑戰(zhàn)了“形態(tài)控制生物可利用性”的傳統(tǒng)認(rèn)知。
3. 低分子量硫醇(LMM-RSH)濃度(表1、圖3)
數(shù)據(jù)來源:LC-ESI-MS測(cè)定10種LMM-RSH(如半胱氨酸、谷胱甘肽)。
結(jié)果:生物源硫醇(半胱氨酸、谷胱甘肽等)濃度與k??顯著正相關(guān)(圖3)。
意義:LMM-RSH可能通過兩種機(jī)制影響甲基化:
動(dòng)力學(xué)控制:調(diào)節(jié)微生物可利用的汞池大小。
微生物活性標(biāo)志:硫醇濃度反映甲基化微生物(如Geobacter)的活性。
4. 其他地球化學(xué)參數(shù)(表1)
關(guān)鍵參數(shù):pH(4.16–6.16)、DOC(18–440 mg L?1)、H?S(<0.15–270 μM)、Fe(II)(0.05–370 μM)。
意義:濕地氧化還原梯度(鐵還原→硫酸鹽還原)為甲基化提供了多樣化的微環(huán)境。
五、結(jié)論
溶解度主導(dǎo)甲基化:孔隙水中溶解態(tài)汞(而非吸附態(tài)汞)的濃度是k??的關(guān)鍵限制因素。
硫醇的間接作用:LMM-RSH(尤其是生物源硫醇)濃度與k??正相關(guān),可能反映微生物活性而非直接調(diào)控汞形態(tài)。
模型局限性:熱力學(xué)形態(tài)模型未能預(yù)測(cè)k??,需結(jié)合微生物活性和動(dòng)力學(xué)過程。
六、丹麥Unisense電極數(shù)據(jù)的詳細(xì)解讀
1. 技術(shù)原理與實(shí)驗(yàn)設(shè)計(jì)
原理:Unisense H?S微電極基于 安培法,通過H?S在電極表面氧化產(chǎn)生電流信號(hào)(檢測(cè)限0.3 μM)。
設(shè)計(jì):
原位測(cè)量:電極直接插入濕地土壤孔隙水,避免采樣擾動(dòng)。
實(shí)時(shí)監(jiān)測(cè):結(jié)合pH電極(Mettler Toledo),同步記錄pH-H?S動(dòng)態(tài)。
2. 關(guān)鍵結(jié)果與生態(tài)意義
H?S濃度范圍:<0.15 μM(鐵還原區(qū))至270 μM(硫酸鹽還原區(qū))(表1)。
意義:
精準(zhǔn)量化硫化物梯度:為熱力學(xué)模型提供高精度H?S(aq)數(shù)據(jù)(pH<7時(shí)H?S為主要硫形態(tài))。
揭示氧化還原分區(qū):H?S與Fe(II)濃度負(fù)相關(guān)(R2=0.76),明確硫酸鹽還原與鐵還原的競(jìng)爭(zhēng)關(guān)系。
支持模型驗(yàn)證:35個(gè)樣本H?S<0.3 μM(設(shè)為0.15 μM),確保模型在低硫條件下的可靠性。
3. 對(duì)甲基化研究的貢獻(xiàn)
排除硫化物干擾:證實(shí)低H?S樣本中甲基化仍可發(fā)生(如鐵還原區(qū)),暗示硫化物非唯一甲基化驅(qū)動(dòng)力。
輔助形態(tài)計(jì)算:H?S數(shù)據(jù)直接輸入熱力學(xué)模型,計(jì)算Hg(SH)?(aq)等形態(tài)(圖2),盡管其與k??無直接關(guān)聯(lián)。
總結(jié)
本研究通過多尺度分析,明確了北方濕地中汞溶解度與生物源硫醇共同調(diào)控甲基汞形成的雙重機(jī)制。丹麥Unisense電極的應(yīng)用為原位硫化物監(jiān)測(cè)提供了高精度數(shù)據(jù),深化了對(duì)濕地氧化還原梯度的理解,但研究也揭示熱力學(xué)模型在預(yù)測(cè)生物過程時(shí)的局限性,未來需整合微生物組學(xué)與動(dòng)力學(xué)模型。