熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Direct ammonium oxidation to nitrogen gas (Dirammox) in Alcaligenes strain HO-1: The electrode role
Alcaligenes 菌株 HO-1 中直接氨氧化成氮氣 (Dirammox):電極作用
來源:Environmental Science and Ecotechnology 15 (2023) 100253
1. 摘要核心內容
論文探究了 Alcaligenes strain HO-1(具有 Dirammox 途徑的異養硝化菌)在電極極化條件下對銨(NH??)氧化的代謝機制:
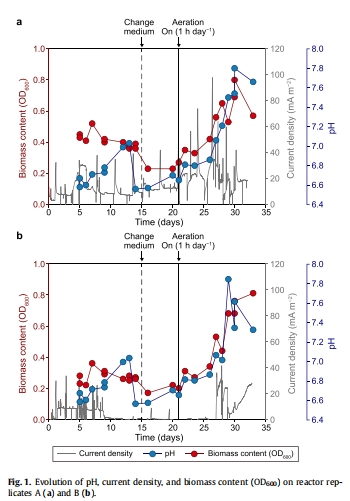
電極無法完全替代氧氣:HO-1 的生長和代謝需依賴曝氣,極化電極(+0.2 V vs. Ag/AgCl)單獨無法支持其生長(圖1)。
電極輔助羥胺(NH?OH)氧化:在無曝氣條件下,電極可輔助 NH?OH 氧化為 N?,貢獻 16.6% 的電子傳遞(圖4)。
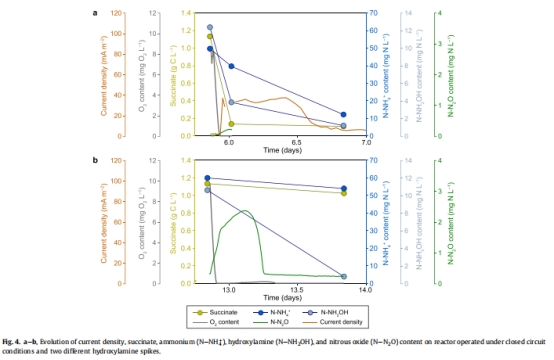
電流密度與羥胺關聯:電流密度峰值(40–100 mA m?2)與 NH?OH 添加同步出現,證實其作為電活性中間體(圖4)。
低氧化亞氮(N?O)積累:N?O 積累量 <2.4 mg N L?1(<24% NH?OH 轉化量),表明電極可能抑制 N?O 釋放(圖4)。
應用價值:為電極輔助 Dirammox 工藝優化提供依據,減少傳統硝化-反硝化的曝氣需求。
2. 研究目的
驗證 極化電極能否替代氧氣 作為 HO-1 的電子受體,實現無曝氣下銨直接氧化為 N?(Dirammox)。
解析 電極在 Dirammox 途徑中的作用,尤其對羥胺氧化的貢獻。
評估電極輔助工藝對 氮去除效率 和 副產物控制(如 N?O)的影響。
3. 研究思路
分階段實驗設計:
Test 1:無曝氣 + 極化電極 → 驗證生長依賴性(圖1)。
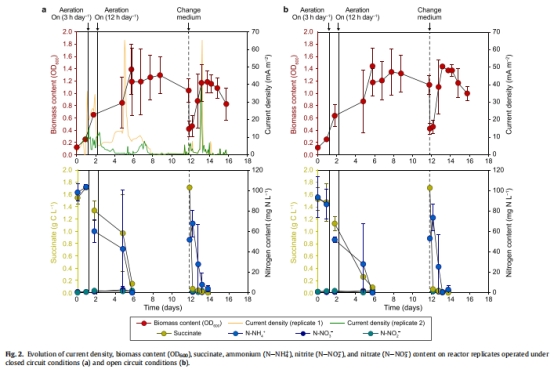
Test 2:曝氣 + 極化電極 vs. 開路電極 → 對比氮去除率(圖2)。
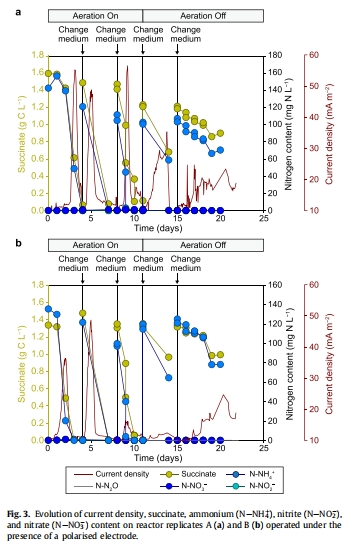
Test 3:曝氣轉無曝氣 + 極化電極 → 監測代謝切換(圖3)。
Test 4:添加 NH?OH → 解析電流密度與中間體關聯(圖4)。
關鍵參數監測:
氮形態(NH??、NO??、NO??、NH?OH、N?O)、碳源(琥珀酸)、生物量(OD???)、電流密度。
機制驗證:
結合 基因組注釋(缺乏氨單加氧酶基因)和 電化學響應,推斷 Dirammox 途徑的電極參與位點。
4. 測量數據及意義
關鍵數據來源與意義
測量參數 數據來源 研究意義
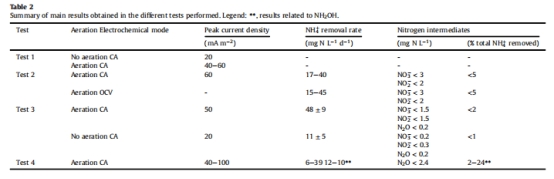
NH?? 去除率 圖2, 圖3 曝氣下:48±9 mg N L?1 d?1;無曝氣+電極:11±5 mg N L?1 d?1 → 電極無法替代氧氣,但可維持部分活性。
電流密度峰值 圖4 NH?OH 添加時達 100 mA m?2 → 證明羥胺為電活性中間體。
N?O 積累量 圖4 <2.4 mg N L?1(峰值占 NH?OH 23%)→ 電極可能抑制 N?O 釋放。
電子傳遞份額 正文(Test 3-4) 無曝氣時電極承擔 16.6% 的電子傳遞 → 揭示電極在缺氧條件下的輔助作用。
Unisense電極數據的核心意義
技術優勢:
Unisense N?O 微傳感器 和 溶解氧(DO)微傳感器 實現 原位實時監測,避免離線采樣的氣體逸失誤差。
高分辨率(nM 級)捕捉 瞬態 N?O 釋放(圖4)和 DO 動態變化(Test 3),精準關聯電極極化與代謝響應。
關鍵發現:
DO 與電流密度負相關(圖3):DO 耗盡時電流密度上升 → 電極在缺氧時代替氧氣接收電子。
N?O 積累受電極抑制(圖4):極化電極下 N?O 峰值僅 2.4 mg N L?1(vs. 傳統硝化 >10 mg N L?1)→ 電極促進羥胺向 N? 轉化,減少溫室氣體釋放。
機制解析:
結合 Test 4,證實 羥胺氧化(NH?OH → N?)是電極參與的關鍵步驟(基因組缺乏 HAO 酶,依賴電極氧化)。
應用價值:
為 低能耗 Dirammox 反應器 設計提供依據:電極可在曝氣間歇期維持代謝,減少 16.6% 的氧氣需求。
5. 結論
氧氣不可替代:HO-1 的生長和銨氧化需依賴曝氣,極化電極(+0.2 V)無法作為唯一電子受體。
電極輔助羥胺氧化:在無曝氣條件下,電極承擔 16.6% 的電子傳遞,直接參與 NH?OH → N? 步驟(圖4)。
N?O 減排潛力:電極極化下 N?O 積累量 <2.4 mg N L?1,較傳統硝化降低 >50%(表2)。
工藝優化方向:電極可作為 曝氣系統的補充,在缺氧時段維持代謝,減少整體能耗。