熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Thioglucose-derived tetrasulfide, a unique polysulfide model compound
硫代葡萄糖衍生的四硫化物:一種獨特的聚硫化物模型化合物
來源:Redox Biology 70 (2024) 103045
氧化還原生物學
摘要內容
摘要指出聚硫化物(RSSnSR, n≥1)在氧化還原生物學中因作為H?S和過硫化物前體而受到關注,但現有生物研究工具主要局限于半胱氨酸和谷胱甘肽衍生的聚硫化物。本研究首次報道了一種基于碳水化合物的新型聚硫化物——硫代葡萄糖四硫化物(TGS4)。該化合物具有優異的水溶性和穩定性,實驗證明其可釋放H?S和過硫化物,并表現出抗氧化活性。細胞實驗顯示TGS4能顯著提升細胞內硫烷硫水平(尤其是過硫化物/三硫化物),表明其是聚硫化物研究的有效工具。
研究目的
開發一種新型碳水化合物基聚硫化物模型(TGS4),以解決現有聚硫化物模型(如半胱氨酸/谷胱甘肽衍生物)的局限性,拓展其在生物學研究中的應用潛力。
研究思路
合成與表征:以β-1-硫代葡萄糖為原料,通過S?Cl?反應一步合成TGS4及其乙酰化衍生物(OAc-TGS4),并通過NMR、質譜和單晶X射線衍射(OAc-TGS4)確認結構。
穩定性評估:測試TGS4在水溶液、有機溶劑及含硫醇標記試劑(IAM/NEM)環境中的穩定性。
功能驗證:
H?S釋放能力:在硫醇(GSH、Cys、Hcy、NAC、BSA蛋白)觸發下定量檢測H?S釋放。
過硫化物生成:驗證其誘導蛋白質過硫化(如GAPDH)及抗氧化活性。
細胞實驗:評估細胞毒性、跨膜能力及對細胞內硫代謝物的影響。
生物學意義探索:通過硫代謝組學分析TGS4對細胞內過硫化物/三硫化物水平的調控作用。
測量的數據及研究意義
H?S釋放動力學(圖2, 3)
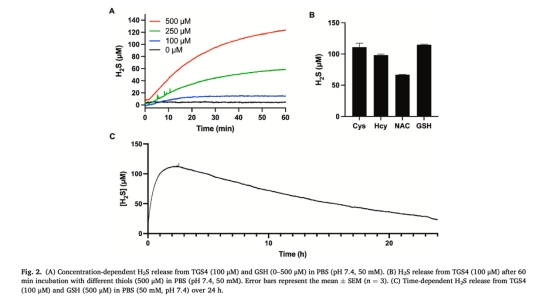
數據:使用Unisense H?S微傳感器實時監測TGS4在不同硫醇(GSH、Cys、Hcy、NAC、BSA)觸發下的H?S釋放濃度隨時間變化。
意義:證明TGS4是高效的H?S供體,尤其在生理濃度GSH(mM級)或蛋白質硫醇(BSA)存在時釋放更顯著,為理解其在生物環境中的行為提供依據。
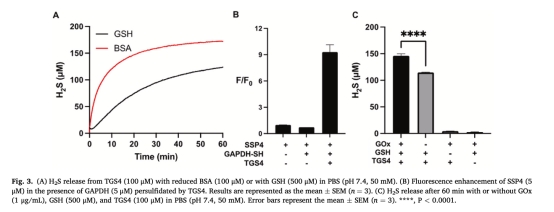
蛋白質過硫化作用(圖3B)
數據:用熒光探針SSP4檢測TGS4處理的GAPDH蛋白的過硫化水平(熒光強度變化)。
意義:證實TGS4能誘導蛋白質翻譯后修飾(S-過硫化),拓展其在硫信號傳導研究中的應用價值。
抗氧化活性(圖4)
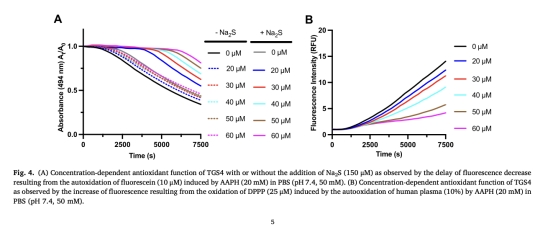
數據:
熒光素氧化抑制實驗:監測AAPH誘導的熒光素吸光度衰減延遲(494 nm)。
血漿脂質過氧化抑制:通過DPPP熒光探針檢測脂質過氧化物生成量。
意義:揭示TGS4通過生成過硫化物(RSSH)發揮抗氧化功能,為開發抗氧化劑提供新思路。
細胞硫代謝組學(圖6)
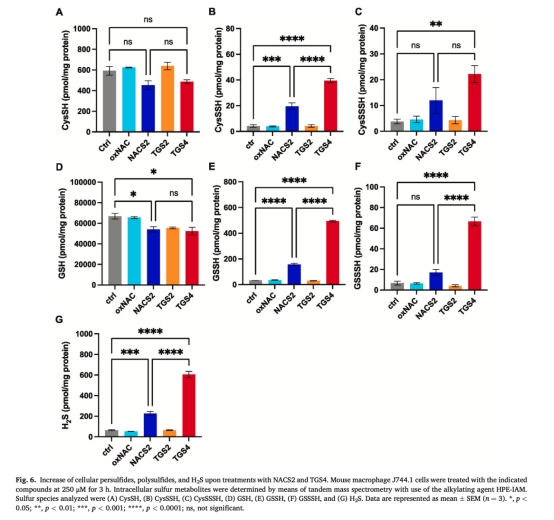
數據:LC-MS/MS定量分析TGS4處理的細胞中硫代謝物(如CysSSH、CysSSSH、GSSH、GSSSH、H?S)水平變化。
意義:首次證明碳水化合物基聚硫化物可高效提升細胞內源性過硫化物/三硫化物水平,且效果優于傳統聚硫化物(如NACS2),為調控細胞氧化還原平衡提供新工具。
丹麥Unisense電極測量數據的研究意義
Unisense H?S微傳感器實時監測的數據(圖2A, 2C, 3A, 3C)具有以下核心價值:
精確動力學解析:揭示TGS4的H?S釋放具有"緩釋"特性(持續>2小時),區別于傳統快速釋放型供體,更貼近生理性H?S生成模式。
硫醇依賴性驗證:量化不同硫醇(小分子/蛋白質)對H?S釋放效率的影響,證明BSA蛋白硫醇的觸發效率高于GSH(圖3A),為理解聚硫化物在血液系統中的行為提供關鍵證據。
協同效應發現:結合葡萄糖氧化酶(GOx)實驗(圖3C),證實TGS4降解產物硫代葡萄糖可被GOx進一步轉化為H?S,深化對碳水化合物基硫化物代謝路徑的認識。
結論
成功開發首個基于碳水化合物的聚硫化物模型TGS4,其合成簡便、水溶性好、穩定性適中。
TGS4可作為高效H?S/過硫化物供體,其釋放行為受硫醇類型和濃度調控,且在蛋白質環境中活性顯著。
具有顯著抗氧化能力,并能誘導細胞硫烷硫水平升高(尤其是過硫化物/三硫化物)。
低細胞毒性且能通過葡萄糖轉運體跨膜,結合獨特的代謝特性(如GOx協同作用),為氧化還原生物學研究提供了優于傳統氨基酸基聚硫化物的新工具。